题目内容
9.为了检验氯化亚铁溶液是否变质,最好向溶液中加入( )| A. | 铁片 | B. | 氢氧化钠溶液 | C. | KSCN溶液 | D. | 石蕊溶液 |
分析 先考虑如果FeCl2溶液变质,变质后的物质是FeCl3,Fe3+能和SCN-生成络合物,使溶液呈现血红色,以此解答该题.
解答 解:FeCl2溶液变质,是由于亚铁离子有强还原性,被氧气氧化为FeCl3,即检验某氯化亚铁溶液是否变质,即是检验是否有Fe3+.而Fe3+能和SCN-生成络合物,使溶液呈现血红色.
故选C.
点评 本题考查了铁离子、亚铁离子的检验方法,为高频考点,侧重考查学生的分析能力,题目难度不大,注意掌握检验Fe3+的试剂:KSCN(溶液变血红色)、苯酚(溶液呈紫色).

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
19.在容积不变的密闭容器中存在如下反应:2A(g)+B(s)?2C(g)△H<0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )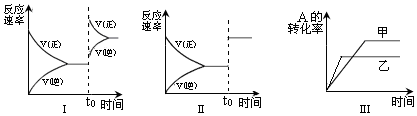

| A. | 图I研究的是t0时刻增大A的浓度对反应速率的影响 | |
| B. | 图II研究的是t0时刻加入催化剂或通入氦气使压强增大后对反应速率的影响 | |
| C. | 图III研究的是催化剂对平衡的影响,且甲的催化效率比乙高 | |
| D. | 图III研究的是温度对化学平衡的影响,且乙的温度较高 |
20.德国化学家F.Haber利用N2和 H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用 、
、 、
、 分别表示N2、H2、NH3,下列说法正确的是( )
分别表示N2、H2、NH3,下列说法正确的是( )

 、
、 、
、 分别表示N2、H2、NH3,下列说法正确的是( )
分别表示N2、H2、NH3,下列说法正确的是( )
| A. | 催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键 | |
| B. | 在该过程中,N2、H2断键形成N原子和H原子 | |
| C. | 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量 | |
| D. | 使用催化剂,合成氨反应放出的热量减少 |
4.下列说法正确的是( )
| A. | 只含H、N、O三种元素的化合物,可能是离子化含物,也可能是共价化合物 | |
| B. | 元素周期表中,ⅠA族与ⅦA族元素间只能形成离子化合物 | |
| C. | NaHCO3、CH3COONa均含有离子键和共价键 | |
| D. | 化合物MgO、SiO2、SO3中化学键的类型相同 |
14.下列有关化学用语表示正确的是( )
| A. | H2O的结构式:H═O═H | B. | F-的结构示意图: | ||
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | D. | NH3的电子式: |
1.利用下列实验装置能完成相应实验的是( )
| A. |  制取并收集干燥纯净的NH3 | B. |  模拟海水蒸馏 | ||
| C. |  收集NO2气体 | D. |  包有足量Na2O2的脱脂面燃烧 |
18.工业废水中常含有不同类型的污染物,可采用不同的方法处理.以下处理措施和方法类别都正确的是( )
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 含Cr2O72-废水 | 加FeSO4沉降 | 物理法 |
| B | 含纯碱的废水 | 加石灰水反应 | 化学法 |
| C | 含Cu2+等重金属离子的废水 | 加硫酸盐沉降 | 化学法 |
| D | 含复杂有机物的废水 | 通过微生物代谢 | 生物法 |
| A. | A | B. | B | C. | C | D. | D |
2. 一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.有关说法错误的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.有关说法错误的是( )
 一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.有关说法错误的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.有关说法错误的是( )| A. | 中间室Cl-移向左室 | |
| B. | 反应后将左右两室溶液混合比反应前将两室溶液混合的酸性强 | |
| C. | 气体X为CO2 | |
| D. | 左边离子交换膜为氯离子交换膜,右边离子交换膜为钠离子交换膜 |