题目内容
下列叙述中正确的是( )
| A、向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体 |
| B、能使润湿的淀粉KI试纸变成蓝色的物质一定是C12 |
| C、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D、HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 |
考点:胶体的重要性质,不同晶体的结构微粒及微粒间作用力的区别,物质的检验和鉴别的基本方法选择及应用
专题:
分析:A.向沸水中逐滴加入少量饱和FeCl3溶液,氯化铁水解可生成氢氧化铁胶体;
B.能使润湿的淀粉KI试纸变成蓝色的物质应具有氧化性;
C.碘离子为无色,振荡静置后CCl4层显紫色,说明溶液中存在碘单质;
D.由阳离子、阴离子离子构成的化合物化合物是离子化合物,一般由活泼金属和活泼非金属元素组成.
B.能使润湿的淀粉KI试纸变成蓝色的物质应具有氧化性;
C.碘离子为无色,振荡静置后CCl4层显紫色,说明溶液中存在碘单质;
D.由阳离子、阴离子离子构成的化合物化合物是离子化合物,一般由活泼金属和活泼非金属元素组成.
解答:
解:A.向沸水中逐滴加入少量饱和FeCl3溶液,氯化铁水解可生成氢氧化铁胶体,故A正确;
B.能使润湿的淀粉KI试纸变成蓝色的物质应具有氧化性,不一定为氯气,故B错误;
C.碘离子为无色,振荡静置后CCl4层显紫色,说明溶液中存在碘单质,故C错误;
D.NaCl是离子化合物,但氯化氢是共价化合物,故D错误.
故选A.
B.能使润湿的淀粉KI试纸变成蓝色的物质应具有氧化性,不一定为氯气,故B错误;
C.碘离子为无色,振荡静置后CCl4层显紫色,说明溶液中存在碘单质,故C错误;
D.NaCl是离子化合物,但氯化氢是共价化合物,故D错误.
故选A.
点评:本题考查较为综合,多角度考查元素化合物知识,为高考常见题型,侧重于学生的分析能力的考查,难度中等,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关实验操作的叙述中,合理的是( )
| A、把SO2通入紫色石蕊试液,可验证SO2的漂白性 |
| B、中和滴定前,用待测液润洗锥形瓶 |
| C、将10g CuSO4?5H2O溶解在90g水中配制10%的CuSO4溶液 |
| D、配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高 |
能够用来鉴别乙醇、乙酸和苯的物质是( )
| A、紫色石蕊试液 | B、氢氧化钠溶液 |
| C、金属钠 | D、水 |
在H2O中加入等物质的量的Ag+、Na+、Ba2+、NO3-、SO42-、Cl-,该溶液在惰性电极的电解槽中通电片刻后,氧化产物和还原产物的质量比是( )
| A、1:2 |
| B、8:1 |
| C、35.5:108 |
| D、108:35.5 |
能证明淀粉已经完全水解的试剂是( )
| A、碘化钾溶液 | B、银氨溶液 |
| C、碘水 | D、酚酞试剂 |

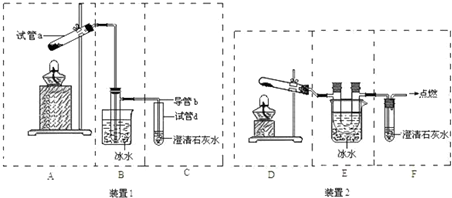
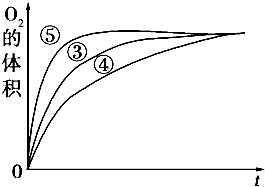 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.