题目内容
4.下列装置(夹持装置略去)能达到实验目的是( )| 选项 | A | B | C | D |
| 装置 | 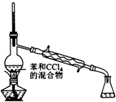 | 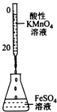 | 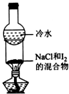 | 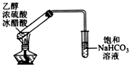 |
| 实验目的 | 分离苯和CCl4 | 酸性KmnO4溶液滴定FeSO4溶液 | 除去NaCl中的I2 | 制备和收集少量乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.蒸馏时不能用球形冷凝管;
B.高锰酸钾应用酸式滴定管盛放;
C.碘易升华;
D.应防止倒吸,且用饱和碳酸钠溶液.
解答 解:A.直形冷凝管一般是用于蒸馏,即在用蒸馏法分离物质时使用,而球形冷凝管一般用于反应装置,即在反应时考虑到反应物的蒸发流失而用球形冷凝管冷凝回流,使反应更彻底,故A错误;
B.高锰酸钾具有腐蚀性,可腐蚀橡胶管,应用酸式滴定管盛放,故B错误;
C.氯化钠性质稳定,且熔点高,碘易升华,可用加热的方法除去,故C正确;
D.导管末端不能插入液面一下,防止倒吸,且应用饱和碳酸钠溶液,故D错误.
故选C.
点评 本题考查较为综合,涉及物质的分离、中和滴定以及乙酸乙酯的制备等知识,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力和评价能力的考查,注意把握实验操作要点以及实验的严密性和可行性的评价,易错点为A,难度中等.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
14.有a、b、c、d四种元素,原子序数依次增大.a存在a+和a-两种离子,b和c为短周期同一主族元素,c的次外层有8个电子,c2-和d2+的电子层结构相同.下列叙述正确的是( )
| A. | b和c分别与a形成化合物的相对分子质量一定为b>c | |
| B. | a和d形成的化合物与水反应产生的气体可做燃料 | |
| C. | +6价的c和a、b形成离子化合物 | |
| D. | a、b、c和d四种元素组成的化合物的水溶液加入少量Na2CO3只产生气体,不产生沉淀 |
12.X、Y、Z、W、M均为短周期元素,X、Y处于同一周期,Z、W处于同一周期,X、Y 原子最外层电子数之和等于Z、W 原子最外层电子数之和,Y 是形成化合物种类最多的元素,X、W 的简单离子X2-、W3+具有相同的电子层结构,M为短周期中除稀有气体元素外原子半径最大的元素.下列说法正确的是( )
| A. | X最高价氧化物对应的水化物为强酸 | |
| B. | 原子半径大小顺序为M>W>X>Y>Z | |
| C. | 水溶液中Z 的简单单核离子能促进水的电离 | |
| D. | Z、M的最高价氧化物对应的水化物均能溶解W与X形成的化合物 |
16.一定条件下,A、B、C、D 之间的转化关系如图所示.下列说法正确的是( )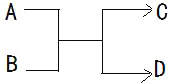

| A. | 若 A 为铁,D 为氢气,则 B 一定为酸 | |
| B. | 若 A、D 为化合物,B 为水,则 C 一定是气体单质 | |
| C. | 若 A、B、C、D 均为化合物,该反应一定属于复分解反应 | |
| D. | 若 A、B、C、D 均为 10 电子微粒,且 C 是可使湿润的红色石蕊试纸变蓝的气体,则 D 常温下一定呈液态 |
13.如表叙述不正确的是( )
| A | B | C | D |
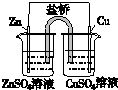 | 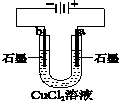 |  |  |
| 盐桥中的Cl-移向ZnSO4溶液 | a极附近产生的气体能使湿润的淀粉碘化钾试纸变蓝 | 粗铜的电极反应式为:Cu2++2e-=Cu | 正极反应式为: O2+4e-+2H2O=4OH- |
| A. | A | B. | B | C. | C | D. | D |
14.下列实验设计正确的是( )
| A. | 将SO2通入溴水中证明SO2具有漂白性 | |
| B. | 将铁屑放入稀HNO3中证明Fe比H2活泼 | |
| C. | 将澄清石灰水滴入某溶液证明其中存在CO32- | |
| D. | 将乙烯通入KMnO4酸性溶液证明乙烯具有还原性 |
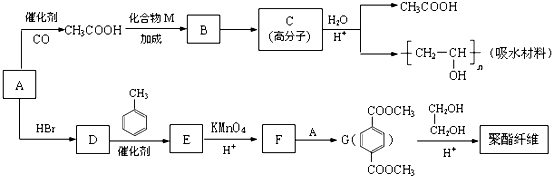
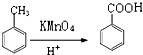
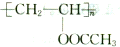 ,D→E的反应类型是取代反应.
,D→E的反应类型是取代反应. .
.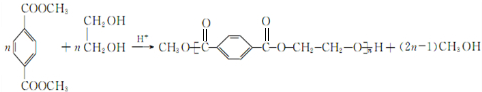 .
. (写结构简式)
(写结构简式)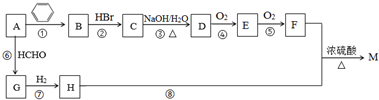
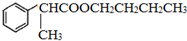 .B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为
.B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为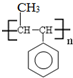 .
.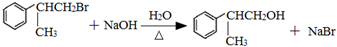 .
.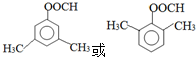 (任写一种物质的结构简式).
(任写一种物质的结构简式).