题目内容
3. 下图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
下图曲线a表示反应X(g)+Y(g)+N(s)?Z(g)+M(g)△H<0进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )| A. | 升高温度 | B. | 加大N的投入量 | C. | 添加催化剂 | D. | 加大X的投入量 |
分析 由图象可知,由曲线a到曲线b,到达平衡的时间缩短,故改变条件,应反应速率加快,且平衡时x的转化率不变,说明条件改变不影响平衡状态的移动,据此结合选项判断.
解答 解:由图象可知,由曲线a到曲线b,到达平衡的时间缩短,故应改变条件使反应速率加快,且平衡时x的转化率不变,说明条件改变不影响平衡状态的移动,故可通过加催化剂或增大压强(必须是反应前后气体体积不变的反应)来实现.
A、该反应正反应是放热反应,升高温度,反应速率加快,平衡向逆反应移动,x的转化率降低,故A错误;
B、N是固体,加大N的投入量,不影响化学反应速率,反应不会加快,故B错误;
C、添加催化剂,化学反应速率加快,达平衡时间缩短,但平衡不移动,故C正确;
D、加大X的投入量,X浓度增大,反应速率加快,平衡向正反应移动,但X的转化率降低,故D错误.
故选:C.
点评 本题考查化学平衡图象、影响平衡移动的因素等,难度不大,根据图象判断条件改变增大反应速率但平衡不移动是解题的关键.

练习册系列答案
相关题目
14.设NA为可伏加德罗常数的值,则下列说法正确的是( )
| A. | 标准状况下,4.48LCH3Cl中含有的原子数为NA | |
| B. | 常温常压下,14 g N2含有的核外电子数为5NA | |
| C. | 10L PH=1的硫酸中含有的氢离子数为2 NA | |
| D. | 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数为2NA |
11.下列说法正确的是( )
| A. | 1 mol C7H16中含有23 mol共价键 | |
| B. | 标准状况下1.12 L NH3中含有0.5 mol e- | |
| C. | 常温常压下0.37g 2H35Cl中含有0.2mol中子 | |
| D. | 40 g NaOH 溶于1 L水,所得溶液中c(Na+)=1 mol•L-1 |
18.可逆反应mA(s)+nB(g)?pC(g)+qD(g)△H=Q kJ•mol-1在反应过程中,当其它条件不变时,C的体积分数Φ(C)在不同温度(T)和不同压强(P)的条件下随时间(t)的变化关系如图所示.下列叙述正确的是( )
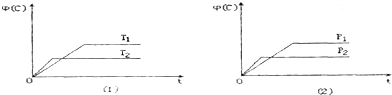

| A. | T1>T2 P1>P2 | B. | Q>0 | ||
| C. | m+n<p+q | D. | 该反应一定具有自发性 |
8.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)═CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
回答下列问题:
(1)该反应为吸热反应(填“吸热”、“放热”),写出该反应的平衡常数表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是bc.
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3)能判断该反应是否达到化学平衡状态的依据是bc.
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)若在(4)所处的温度下,在1L的密闭容器中,加入2molCO2和3molH2充分反应达平衡时,H2的物质的量为b,CO2的物质的量为c.
a.等于1.0mol b.大于1.0mol c.大于0.5mol,小于1.0mol d.无法确定.
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为吸热反应(填“吸热”、“放热”),写出该反应的平衡常数表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是bc.
a.及时分离出CO气体 b.适当升高温度
c.增大CO2的浓度 d.选择高效催化剂
(3)能判断该反应是否达到化学平衡状态的依据是bc.
a.容器中压强不变 b.混合气体中 c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为830℃.
(5)若在(4)所处的温度下,在1L的密闭容器中,加入2molCO2和3molH2充分反应达平衡时,H2的物质的量为b,CO2的物质的量为c.
a.等于1.0mol b.大于1.0mol c.大于0.5mol,小于1.0mol d.无法确定.
15.3.2g Cu与30mL 3mol•L-1HNO3溶液充分反应,还原产物有NO2和NO,若反应后溶液中H+为a mol,则此时溶液中所含NO3-为( )
| A. | $\frac{a}{2}$ mol | B. | 2a mol | C. | 0.1a mol | D. | (a+0.1)mol |
3.下列图示与对应的叙述相符的是( )
| A. | 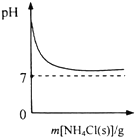 表示向NH3•H2O溶液中逐步加入NH4Cl固体后,溶液pH的变化 | |
| B. | 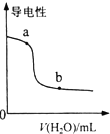 表示向NH3•H2O溶液中加水时溶液的导电性变化,则NH3•H2O溶液的pH:b>a | |
| C. | 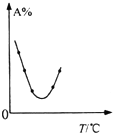 表示等量A在容积相同的恒容密闭容器中,不同温度下分别发生反应:2A(g)?B(g)+C(g),相同时间后测得A含量的曲线,则该反应的△H<0 | |
| D. | 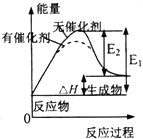 表示催化剂能改变化学反应的焓变 |
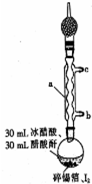 四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下:
四碘化锡是一种橙红色结晶,熔点为144.5℃,沸点为364℃,不溶于冷水,溶于醇、苯、氯仿等,遇水易水解,常用作分析试剂和有机合成试剂.实验室制备四碘化锡的主要步骤如下: