题目内容
Na、Mg、Al各2mol,分别与含1mol HCl的盐酸反应,在相同状况下产生的H2的体积之比为( )
| A、1:1:1 |
| B、1:2:3 |
| C、2:1:1 |
| D、3:2:1 |
考点:离子方程式的有关计算
专题:
分析:Na能与酸、水反应生成氢气,根据电子转移守恒计算生成氢气的物质的量,而Mg、Al只能与酸反应,不能与水反应,进行过量计算,根据不足量的物质计算生成氢气的物质的量,相同条件下,气体体积之比等于其物质的量之比.
解答:
解:三种金属与酸反应的方程式分别为2Na+2HCl=2NaCl+H2↑、Mg+2HCl=MgCl2+H2↑、2Al+6HCl=2AlCl3+3H2↑,
将Na,Mg,Al各2mol分别投入到含1mol HCl的盐酸中,根据方程式知,2molMg完全反应消耗4molHCl、2molAl完全反应消耗6molHCl,Na能和水反应,所以Mg、Al不能完全反应,2molNa完全反应生成氢气的物质的量为
=1mol,Mg、Al和盐酸反应时金属过量,应按照盐酸计算,则生成氢气的物质的量都是0.5mol,相同条件下,气体的体积之比等于其物质的量之比,所以Na、Mg、Al分别生成的氢气体积之比=1mol:0.5mol:0.5mol=2:1:1,
故选C.
将Na,Mg,Al各2mol分别投入到含1mol HCl的盐酸中,根据方程式知,2molMg完全反应消耗4molHCl、2molAl完全反应消耗6molHCl,Na能和水反应,所以Mg、Al不能完全反应,2molNa完全反应生成氢气的物质的量为
| 2mol |
| 2 |
故选C.
点评:本题以金属和酸反应为载体考查了物质的量的有关计算,明确反应中各个物理量的关系即可解答,题目难度不大.

练习册系列答案
相关题目
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g)?4NO2 (g)+O2(g)△H>0
t℃时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确的是( )
t℃时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确的是( )
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/mol?L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
| A、500 s 内N2O5分解速率为2.96╳10-3mol?L-1?s-1 |
| B、达平衡时,N2O5的转化率为50% |
| C、达平衡后,升高温度平衡常数减小 |
| D、达平衡后,其他条件不变,将容器的体积压缩到原来的一半,c(N2O5)>5.00 mol?L-1 |
下列说法不正确的是( )
A、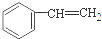 没有顺反异构体 没有顺反异构体 |
| B、1,3-丁二烯可以作为合成高分子化合物的原料 |
| C、用乙醇和浓硫酸制备乙烯时,用水浴加热控制反应温度 |
| D、常温下,将苯酚加入到少量水中有浑浊,滴入适量NaOH溶液后浑浊消失 |
E、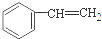 |
向一定量的Fe、FeO、Fe3O4和Fe2O3的混合物中加入250mL 4mol/L的稀硝酸,恰好使混合物完全溶解.放出2.24L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现,若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
| A、0.21mol |
| B、0.25mol |
| C、0.45mol |
| D、0.5mol |
下列各化合物的命名正确的是( )
| A、CH2=CH-CH=CH2 1,3-二丁烯 |
B、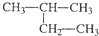 2-甲基丁烷 2-甲基丁烷 |
C、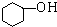 苯酚 苯酚 |
D、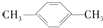 间二甲苯 间二甲苯 |
水的电离过程为H2O?H++OH-,在25℃、35℃时其离子积分别为K(25℃)=1.0×10-14、K(35℃)=2.1×10-14,则下列说法中正确的是( )
| A、水的电离过程是吸热过程 |
| B、c(H+)随着温度的降低而升高 |
| C、在35℃时,纯水中c(H+)>c(OH-) |
| D、水的电离度α(25℃)>α(35℃) |