题目内容
14.工业级氢氧化钾熔液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯,电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示.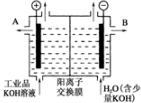
①该电解槽的阳极反应式是4OH--4e-=2H2O+O2↑.
②通电后,阴极附近溶液pH会增大,请简述原因H+放电,促进水的电离,溶液中的OH-浓度增大.
③除去杂质后的 氢氧化钾溶液从液体出口B(填“A”或“B“)导出.
分析 ①用阳离子交换膜电解法除去工业品氢氧化钾溶液中的杂质含氧酸根,相当于电解水,阳极氢氧根离子放电;
②电解时阴极区H+放电,H+浓度减小,使水的电离平衡向右移动促进水的电离,OH-浓度增大;
③在阴极和阳极之间有阳离子交换膜,只允许阳离子K+和H+通过,这样就在阴极区聚集大量的K+和OH-,从而产生纯的氢氧化钾溶液,所以除去杂质后的氢氧化钾溶液从溶液出口在阴极区.
解答 解:①用阳离子交换膜电解法除去工业品氢氧化钾溶液中的杂质含氧酸根,相当于电解水,阳极发生氧化反应,故电解时阳极电极反应式:4OH--4e-=2H2O+O2↑,
故答案为:4OH--4e-=2H2O+O2↑;
②阴极电极反应式:4H++4e-=2H2↑,其中阴极区H+放电,H+浓度减小,使水的电离平衡向右移动促进水的电离,溶液中OH-浓度增大,阴极附近溶液pH会增大,
故答案为:H+放电,促进水的电离,溶液中的OH-浓度增大;
③在阴极区聚集大量的K+和OH-,从而产生纯的氢氧化钾溶液,除杂后的氢氧化钾溶液从出口B导出,
故答案为:B.
点评 本题考查电解原理的应用,关键是根据离子放电顺序判断电解过程中发生的反应,理解除杂原理,题目难度中等.

练习册系列答案
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
4.对于酒精灯火焰由外到里的分布正确的是( )
| A. | 外焰、内焰、焰心 | B. | 外焰、焰心、内焰 | C. | 内焰、焰心、外焰 | D. | 以上均不对 |
5.在下列化学反应中,符合既有离子键、共价键断裂,又有离子键、共价键形成的是( )
| A. | 2 Na2O2+2H2O═4NaOH+O2↑ | B. | 2 Na+2H2O═2NaOH+H2↑ | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$ 2H2O | D. | HCl+NH3═NH4Cl |
2.运用相关化学知识进行判断,下列结论正确的是( )
| A. | 晶体硅硬度大、熔点高,因而可用于制作半导体材料 | |
| B. | 常温下铝制品可以储运浓硫酸和浓硝酸 | |
| C. | 水煤气、液氯、水玻璃、福尔马林为混合物 | |
| D. | 金属汞一旦洒落在实验室地面或桌面上,必须尽快收集,并深埋处理 |
9.下列过程属于物理变化的是( )
| A. | 平行光照射胶体产生丁达尔效应 | B. | 紫外线照射下,液态蛋白质凝固 | ||
| C. | SO2使品红溶液褪色 | D. | 铁遇到冷的浓硝酸溶液发生钝化 |
19.某有机物A分子式为C9H10O2,其水解后产物可以使FeCl3溶液变紫色,则A的同分异构体有( )
| A. | 6种 | B. | 7种 | C. | 13种 | D. | 16种 |
2.对于化学反应能否自发进行,下列说法中错误的是( )
| A. | 若△H>0,△S>0,低温时可自发进行 | |
| B. | 若△H<0,△S<0,低温时可自发进行 | |
| C. | 若△H<0,△S>0,任何温度下都能自发进行 | |
| D. | 若△H>0,△S<0,任何温度下都不能自发进行 |
20.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:-2221.5kJ/mol,下列有关说法正确的是( )
| A. | 奥运火炬燃烧主要是将化学能转变为热能和光能 | |
| B. | 丙烷常温下是液体 | |
| C. | 丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极 | |
| D. | 丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol |