题目内容
(10分)
Ⅰ.向FeCl3溶液中加入铁粉和铜粉混合粉末,充分反应后,下列情况可能存在的是 (填序号)

Ⅱ.今有一包铁粉和铜粉混合粉末,为确定其组成,现提供4mol/L的FeCl3,溶液(其他用品略),某课外活动小组同学的实验结果如下(假定反应前后溶液体积不变)。

(1)试判断第④组剩余固体质量x为 。第①组实验中,发生反应的离子方程式为 。
(2)试判断第②组剩余固体的成分为 。
(3)原混合粉末中Fe、Cu的物质的量之比为 。
(共10分)
Ⅰ.②③⑥⑦(2分,对4个得2分、对3个得1分、对2个或1个、错一个均无分)
Ⅱ.(1) 0 (2分) 2Fe3++ Fe=3Fe2+(2分)
(2)Cu(2分) (3) 6﹕1(2分)
【解析】
试题分析:Ⅰ.①④、在金属活动性顺序中,铁在铜的前面,铁能与铜盐溶液发生置换反应,向装有氯化铁溶液的烧杯中,加入一定量的Cu和Fe的混合粉末,则铁优先与氯化铁发生反应生成氯化亚铁,然后铜与氯化铁反应生成氯化铜和氯化亚铁,故滤液中一定含有氯化亚铁,故①④错误;②③、充分反应后发现有铜剩余,则溶液中一定无氯化铁,一定有FeCl2,可能有CuCl2,故②③正确;⑤若有铁剩余,则溶液中一定不含氯化铜和氯化铁,故⑤错误;⑥充分反应后没有固体剩余,则可能是氯化铁还会剩余,金属量不足的情况,故⑥正确;⑦充分反应后发现铜、铁都存在,则滤液中一定不含有氯化铁、氯化铜,只有氯化亚铁,故⑦正确,所以答案为:②③⑥⑦
Ⅱ.(1)第④组实验,可以看作再第②组实验的基础上再加入50mL FeCl3溶液,发生Cu+2Fe3+=Fe2++Cu2+,50mL溶液可以溶解Cu的质量=0.05L×4mol/L×1/2×64g/mol=6.4g,故x=6.4g-6.4g=0;;第①组实验Fe3+还未反应完,所以发生反应的离子方程式为:2Fe3++ Fe=3Fe2+
(2)铁的还原性强于铜,所以Fe3+先和铁反应:Fe+2Fe3+=3Fe2+,反应完全后Fe3+有剩余,再与铜发生反应:Cu+2Fe3+=Fe2++Cu2+,能剩余的固体可以是铜,可以是铁和铜,第②组实验中,有固体剩余,故FeCl3溶液全部参与反应,若只发生Fe+2Fe3+=3Fe2+,可以溶解Fe的质量为0.3L×4mol/L×1/2×56g/mol=33.6g,300mL FeCl3溶液能溶解金属质量40g-6.4g=33.6g,第③组实验,可以看作再第②组实验的基础上再加入30mL FeCl3溶液,实际溶解金属质量=6.4g-2.56g=3.84g,若只发生Fe+2Fe3+=3Fe2+,30mL溶液可以溶解Fe的质量为0.03L×4mol/L×1/2×56g/mol=3.36g,若只发生Cu+2Fe3+=Fe2++Cu2+,30mL溶液可以溶解Cu的质量为0.03L×4mol/L×1/2×64g/mol=3.84g,可推断第②组实验中Fe恰好反应完全,剩余固体为Cu
(3)根据(1)中分析可知Cu为6.4g,Fe的质量=40g-6.4g=33.6g,故n(Fe)=33.g÷56g/mol=0.6mol,n(Cu)=6.4g÷64g/mol==0.1mol,原混合粉末中Fe、Cu的物质的量之比=0.6mol:0.1mol=6:1。
考点:本题考查氧化还原反应原理及反应顺序、混合物的计算、离子方程式的书写。

已知下列物质的名称分别是
名称 | 硫代硫酸钠 | 多硫化钙 | 过氧化钡 | 超氧化钾 |
化学式 | Na2S2O3 | CaSx | BaO2 | KO2 |
根据上述命名规律回答:K2CS3应命名为
A.三硫代碳酸钾 B.多硫碳酸钾 C.过硫碳酸钾 D.超硫碳酸钾
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:
X2(g) + 3Y2(g) 2XY3(g) △H=-92.6 kJ.mol-1
2XY3(g) △H=-92.6 kJ.mol-1
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化 | ||
X2 | Y2 | XY3 | |||
① | 1 | 3 | 0 | 2分钟 | 放热46.3kJ |
② | 0.4 | 1.2 | 1.2 | / | Q(Q>0) |
下列叙述不正确的是
A.容器①中反应从开始到刚达平衡时用XY3表示的反应速率为v(XY3)=1/30 moI.L-l·s-1
B.平衡时,两个容器中XY3的物质的量浓度相等
C.容器②中反应达到平衡时吸收的热量为Q
D.容器①体积为0.3L,则达平衡时放出的热量大于46.3kJ
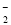 +2H2O
+2H2O