题目内容
9.在一固定容积的密闭容器中,可逆反应N2+3H2?2NH3达到平衡状态的标志是( )| A. | v(N2)正=v(NH3)逆 | |
| B. | 单位时间内3molH-H键断裂,同时6molN-H键断裂 | |
| C. | n(N2):n(H2):(NH3)=1:3:2 | |
| D. | 混合气体的密度不再改变 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、速率之比不等计量数之比,所以不是平衡状态,故A错误;
B、单位时间内3molH-H键断裂等效于6molN-H键形成,同时6molN-H键断裂,所以正逆反应速率相等达平衡状态,故B正确;
C、当体系达平衡状态时,n(N2):n(H2):(NH3)之比可能1:3:2,也可能不等1:3:2,与各物质的初始浓度及转化率有关,故C错误;
D、混合气体的密度一直不变,所以不能说明达平衡状态,故D错误;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、C的化学式:BKNO3;CKAl(SO4)2.
(2)写出过量E滴入到C溶液中的离子反应方程式Al3++4OH-═AlO2-+2H2O.
(3)在A溶液中加澄清石灰水,其离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O.
(4)写出检验D中阴离子的方法取样,先加盐酸,再滴加氯化钡溶液.
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、HCO3-、NO3-、SO42- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、C的化学式:BKNO3;CKAl(SO4)2.
(2)写出过量E滴入到C溶液中的离子反应方程式Al3++4OH-═AlO2-+2H2O.
(3)在A溶液中加澄清石灰水,其离子方程式为HCO3-+Ca2++OH-=CaCO3↓+H2O.
(4)写出检验D中阴离子的方法取样,先加盐酸,再滴加氯化钡溶液.
5.下列物质与NaOH的酚酞溶液共热时,能使溶液颜色褪去的有( )
①乙酸 ②乙醇③乙酸乙酯④氯乙烷.
①乙酸 ②乙醇③乙酸乙酯④氯乙烷.
| A. | ① | B. | ②③ | C. | ②④ | D. | ①③④ |

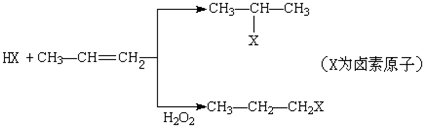
 的物质,该物质是一种香料.
的物质,该物质是一种香料.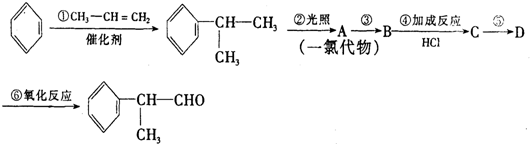
 ,
,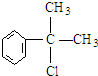 .
.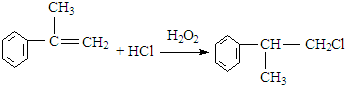 .反应⑤的化学方程式为(有机物写结构简式,并注明反应条件):
.反应⑤的化学方程式为(有机物写结构简式,并注明反应条件):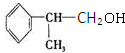 +NaCl.
+NaCl.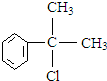 的水解产物
的水解产物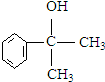 不能经氧化反应⑥而得到产品,导致产率低.
不能经氧化反应⑥而得到产品,导致产率低. ,
, ,
, .
.