题目内容
2.下列关于化学键的叙述,正确的一项是( )| A. | 离子化合物中一定含有离子键 | |
| B. | 单质分子中均存在化学键 | |
| C. | 含有极性键的分子一定是极性分子 | |
| D. | 含有共价键的化合物一定是共价化合物 |
分析 A.含有离子键的化合物是离子化合物;
B.单质分子有的存在化学键,有的不含化学键;
C.含有极性键的分子不一定是极性分子;
D.含有共价键的化合物不一定是共价键化合物.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH中含有离子键和共价键,故A正确;
B.单质分子中有的含有化学键,如H2,有的不含化学键,如稀有气体分子,故B错误;
C.含有极性键的分子不一定是极性分子,如果分子正负电荷重心重合,则就是非极性分子,如CCl4,故C错误;
D.含有共价键的化合物不一定是共价键化合物,可能是离子化合物,如NH4Cl,故D错误;
故选A.
点评 本题考查了化学键和物质的关系,注意不是所有的物质都含有化学键,如稀有气体分子中不含化学键,题目难度不大,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
10.在100mL(Na2CO3)与NaAlO2的混合液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO${\;}_{3}^{2-}$、HCO${\;}_{3}^{-}$、AlO${\;}_{2}^{-}$、Al3+离子的物质的量与加入盐酸溶液的体积变化关系,如图所示.下列说法正确的是( )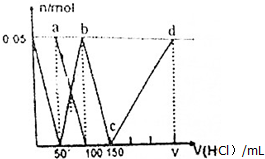

| A. | a点溶液中:c(HCO${\;}_{3}^{-}$)+c(H2CO3)+c(H+)=c(OH-) | |
| B. | 当向混合液中滴加75nL盐酸时,溶液中部分离子浓度大小顺序为:c(Na+)>c(Cl-)>c(CO${\;}_{3}^{2-}$)>c(OH-)>c(H+) | |
| C. | b点溶液中:c(Cl-)+c(HCO3-)+c(H2CO3)+c(CO${\;}_{3}^{2-}$)=1.5mol•L-1 | |
| D. | c→d的过程中水的电离程度逐渐减小 |
13.某化合物XY2的Y-的粒子结构示意图可能是( )
| A. | 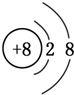 | B. | 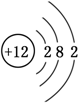 | C. | 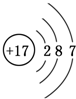 | D. | 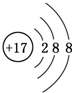 |
10.下列叙述中,与胶体性质无直接关系的是( )
| A. | 含有少量硫的酒精溶液,加入大量水后形成乳白色液体,用滤纸过滤不能分离出硫 | |
| B. | 原硅酸溶液中加入硫酸铵饱和溶液,结果产生沉淀 | |
| C. | 硫酸铜溶液中加入硫化钠溶液产生黑色沉淀 | |
| D. | 用水稀释牛奶,用一束强光照射,从侧面观察,可以看到一条清晰的光路 |
17.下列物质之间的相互关系不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | O2和O3互为同素异形体 | ||
| C. | H、D、T互为同位素 | D. | 干冰和冰为同一种物质 |
7.分离苯和苯酚的混合物,通常采用的方法是( )
| A. | 振荡混合物,用分液漏斗分离 | |
| B. | 加入NaOH溶液后振荡,用分液漏斗分离;取下层液体通入CO2,待分层后分液 | |
| C. | 加水振荡后用分液漏斗分离 | |
| D. | 加稀盐酸振荡后,用分液漏斗分离 |
11.有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如表所示:
下列各项判断正确的是( )
| 第一组 | A-268.8 | B-249.5 | C-185.8 | D-151.7 |
| 第二组 | F2-187.0 | Cl2-33.6 | Br2 58.7 | I2 184.0 |
| 第三组 | HF 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | H2Se 42.0 | H2Te-1.8 |
| A. | 第一组和第二组物质中一定含有共价键 | |
| B. | 第三组与第四组相比较,化合物的稳定顺序为:HBr>H2Se | |
| C. | 第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI | |
| D. | 第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强 |
12.下列每组物质发生变化所克服的粒子间的相互作用属于同种类型的是( )
| A. | 碘和干冰升华 | B. | 氯化钠和冰的熔化 | ||
| C. | 二氧化硅和氧化钠熔化 | D. | 食盐和蔗糖熔化 |
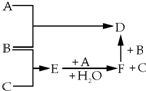 有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.
有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.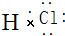 ;
;