题目内容
pH=1的两种一元酸HX和HY的溶液,分别取50mL,加入足量的镁粉,充分反应,收集的氢气的体积分别为V(HX)和V(HY),若V(HX)>V(HY),下列说法正确的是( )
分析:因开始的pH相同,镁足量,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,反应速率与氢离子浓度成正比,以此进行分析并解答.
解答:解:A.pH=l的两种一元酸HX与HY溶液,分别与足量Mg反应,HX产生氢气多,则HX为弱酸,故A正确;
B.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,二者可能一种为强酸,另一种为弱酸,或者二者都是弱酸,其中HX较弱,故B错误;
C.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,故C错误;
D.反应开始时,两种溶液中氢离子浓度相等,所以反应速率相同,故D错误;
故选A.
B.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,二者可能一种为强酸,另一种为弱酸,或者二者都是弱酸,其中HX较弱,故B错误;
C.pH=1的两种一元酸,分别取50mL加入足量镁粉,由V(HX)>V(HY),说明HX溶液的浓度较大,则HX酸性较弱,故C错误;
D.反应开始时,两种溶液中氢离子浓度相等,所以反应速率相同,故D错误;
故选A.
点评:本题考查弱电解质在溶液中的电离,题目难度不大,本题要注意两种酸的强弱比较的角度,不能确定是否一定是强酸.

练习册系列答案
相关题目
pH=1的两种一元酸HX和HY溶液,分别取100mL加入足量的镁粉,充分反应后,收集到H2体积分别为VHX和VHY。若相同条件下VHX>VHY,则下列说法正确的 ( )
| A.HX可能是强酸 | B.HY一定是强酸 |
| C.HX的酸性强于HY的酸性 | D.反应开始时二者生成H2的速率相等 |
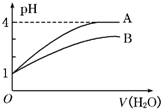 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )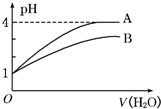 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )