题目内容
构成下列物质的原子不能共平面的是( )
| A、CH4 | B、乙烯 |
| C、乙炔 | D、苯 |
考点:常见有机化合物的结构
专题:有机物分子组成通式的应用规律
分析:根据甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线形分子进行判断原子共面情况;
解答:
解:A.CH4是正四面体结构,最多有3个原子共面,故A错误;
B.乙烯是平面型结构,所有原子都共面,故B正确;
C.乙炔是直线形分子,所有原子都共面,故C正确;
D.苯是平面型结构,所有原子都共面,故D正确;
故选A.
B.乙烯是平面型结构,所有原子都共面,故B正确;
C.乙炔是直线形分子,所有原子都共面,故C正确;
D.苯是平面型结构,所有原子都共面,故D正确;
故选A.
点评:本题考查有机物的空间结构,题目难度不大,注意把握甲烷、乙烯、乙炔和苯的结构特点.

练习册系列答案
相关题目
对于化学反应方向的确定,下列说法正确的是( )
| A、温度、压力一定时,焓变和熵变共同决定一个化学反应的方向 |
| B、温度、压力一定时,放热的熵增加反应不一定能自发进行 |
| C、反应焓变是决定反应能否自发进行的唯一因素 |
| D、固体的溶解过程仅与焓变有关 |
下列物质的分子为手性分子的是( )
| A、CH3COOH |
| B、CH3OH |
| C、CH3CH(F)CHO |
| D、CH3CHO |
“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是( )
| A、活化分子之间的碰撞不一定都是有效碰撞 |
| B、升高温度,可使单位体积内活化分子数增多,反应速率加快 |
| C、催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
| D、对于有气体参加的反应增大压强,可使单位体积内活化分子百分数增加,反应速率加快 |
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A、14g分子通式为CnH2n的链烃中含有的C═C的数目为
| ||
| B、标准状况下,NO和 O2各11.2L 混合,所得混合气体的分子总数为 0.75NA | ||
| C、25℃时,pH=7的NH4Cl和NH3?H2O混合溶液中,OH-离子数为10-7NA | ||
| D、两份2.7g铝分别与100mL浓度为2mol?L-1的盐酸和氢氧化钠溶液充分反应,转移的电子数均为0.3NA |
下列有关物质性质的比较顺序中,不正确的是( )
| A、熔点:F2<Cl2<Br2<I2 |
| B、微粒半径:F->Na+>Mg2+>Al3+ |
| C、酸性HClO4>H2SO4>H3PO4>H2SiO3 |
| D、热稳定性:HF<HCl<HBr<HI |
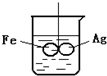 如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心的向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )
如图所示,在铁圈和银圈的焊接处,用一根棉线将其悬在盛水的烧杯中,使之平衡;小心的向烧杯中央滴入CuSO4溶液,片刻后可观察到的现象是( )| A、铁圈和银圈左右摇摆不定 |
| B、保持平衡状态 |
| C、铁圈向下倾斜,银圈向上倾斜 |
| D、银圈向下倾斜,铁圈向上倾斜 |
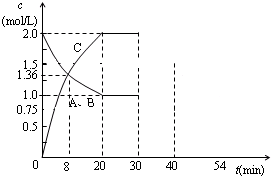 Ⅰ、某容积不变的密闭容器中充入等物质的量的气体A和B,某温度下发生反应:
Ⅰ、某容积不变的密闭容器中充入等物质的量的气体A和B,某温度下发生反应: