题目内容
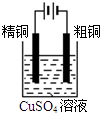
1.下面是两种常见的化学电源示意图,有关说法不正确的是( )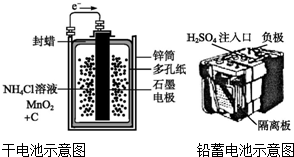
| A. | 上述电池分别属于一次电池、二次电池 | |
| B. | 干电池在长时间使用后,锌筒被破坏 | |
| C. | 铅蓄电池工作过程中,每通过2 mol电子,负极质量减轻207 g | |
| D. | 铅蓄电池负极材料为Pb |
分析 A.干电池是一次性电池,铅蓄电池是可充电电池属于二次电池;
B.干电池中锌做原电池的负极被腐蚀;
C.依据铅蓄电池电极反应结合电子守恒计算;
D.铅蓄电池负极材料为Pb,被氧化生成硫酸铅.
解答 解:A.干电池是一次性电池,铅蓄电池是可充电电池属于二次电池,故A正确;
B.在干电池中,Zn作负极,被氧化,故B正确;
C.铅蓄电池工作过程中,硫酸铅在负极上析出,该极质量应该增加而非减小,故C错误;
D.铅蓄电池负极材料为Pb,被氧化生成硫酸铅,故D正确;
故选C.
点评 本题考查了原电池类型的分析判断,为高频考点,侧重于学生的分析能力的考查,依据原电池原理判断电极和反应产物是解题关键,题目难度中等.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
11.配制一定物质的量浓度的溶液时,如果所配溶液浓度偏小,原因可能是( )
| A. | 转移时没有洗涤2~3次 | |
| B. | 定容时,俯视液面使之与刻度线相平 | |
| C. | 溶解时放出了大量的热,但未等温度恢复为常温就开始转移 | |
| D. | 转移溶液前,容量瓶不干燥,留下少量的水 |
10.向50mL 1mol/L AlCl3溶液中加入1.5mol/L NaOH溶液amL,充分反应后,生成白色沉淀1.56g,则a的数值可能是( )
| A. | 40和120 | B. | 65和90 | C. | 40和90 | D. | 90和120 |
11.下列物质中含有共价键的离子化合物是( )
| A. | CaF2 | B. | KOH | C. | CO2 | D. | CH4 |
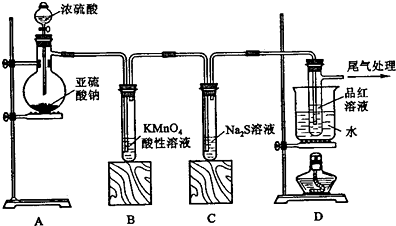
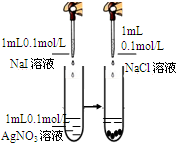

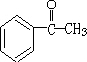
 +NaOH$\stackrel{H_{2}O}{→}$
+NaOH$\stackrel{H_{2}O}{→}$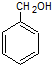 +NaCl,反应类型为取代反应.
+NaCl,反应类型为取代反应. .
. .
.
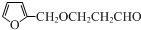


 .
. .
. .
.