题目内容
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2===LiNH2+LiH,下列有关说法正确的是( )
A.Li2NH中N的化合价是-1
B.该反应中H2既是氧化剂又是还原剂
C.Li+和H-的离子半径相等
D.此法储氢和钢瓶储氢的原理相同
B
【解析】
试题解析:A、Li2NH中氮元素的化合价为-3;故A错误;B、反应物H2中的氢元素的化合价为0价,反应后生成LiNH2中H元素的化合价是+1,LiH中H元素的化合价是-1,所以H2既是氧化剂又是还原剂,故B正确;C、Li+核外有一个电子层,H+核外无电子,离子核外电子层数越多,半径越大,故Li+半径大于H+;故C错误;D、钢瓶储氢是物理过程,而该方法为化学方法,故D错误.
考点:氧化还原反应.

 通城学典默写能手系列答案
通城学典默写能手系列答案(12分)A、B、C、D、E为易溶化合物,其离子组成为
阳离子 | Fe3+、Ba2+、Al3+、Na+、Ag+ |
阴离子 | NO3—、OH—、SO42—、Cl—、CO32— |
在各化合物中离子不重复,分别取其溶液进行实验,结果如下:
①在A溶液中逐滴加入氨水,有白色沉淀生成,继续加氨水至过量,沉淀消失;
②用pH试纸测得B和C溶液显碱性,0.1mol/L的C溶液pH小于13;
③在D溶液中加入铁粉,溶液质量增加;④在E溶液中加入过量B,没有沉淀产生。
完成下列填空:
(1)A的化学式为 ;
(2)③反应的离子方程式为 ;
(3)检验D溶液中阴离子的的方法是 ;
(4)E的的化学式为 ,将E蒸干、灼热至质量不再改变,最后所得物质是(填化学式) 。
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
B | Fe3+具有氧化性 | 用KSCN溶液可以鉴别Fe3+ |
C | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
D | SiO2可与HF反应 | 氢氟酸不能保存在玻璃瓶中 |

 +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ AlCl3
AlCl3 Al ② NH3
Al ② NH3 NO
NO HNO3
HNO3 NaHCO3
NaHCO3 Na2CO3 ④FeS2
Na2CO3 ④FeS2 SO3
SO3 H2SO4
H2SO4 与
与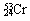 互为同素异形体
互为同素异形体