题目内容
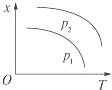 如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是( )
如图表示温度和压强对平衡状态下可逆反应2M(g)+N(g)?2Q(g)△H<0的影响.下列有关说法正确的是( )| A、x不可能是M或N的体积分数 |
| B、x可能是混合气体的物质的量 |
| C、该反应在p1时先达到化学平衡状态 |
| D、p1>p2 |
考点:体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:该反应是反应前后气体体积减小的放热反应,温度不变时,增大压强平衡向正反应方向移动,压强不变时,升高温度,平衡向吸热反应方向移动,据此分析解答.
解答:
解:A.温度不变时,增大压强平衡向正反应方向移动,则M或N的体积分数减小;压强不变时,升高温度,平衡向吸热反应方向移动,M或N的体积分数增大,所以x不可能是M或N的体积分数,故A正确;
B.压强不变时,升高温度,平衡向吸热反应方向移动,平衡向逆反应方向移动,则x不可能是混合气体的物质的量,故B错误;
C.如果x是Q体积分数,增大压强Q体积分数增大,所以p1<p2,则在p2时先达到化学平衡状态,故C错误;
D.如果x是Q体积分数,增大压强Q体积分数增大,所以p1<p2,故D错误;
故选A.
B.压强不变时,升高温度,平衡向吸热反应方向移动,平衡向逆反应方向移动,则x不可能是混合气体的物质的量,故B错误;
C.如果x是Q体积分数,增大压强Q体积分数增大,所以p1<p2,则在p2时先达到化学平衡状态,故C错误;
D.如果x是Q体积分数,增大压强Q体积分数增大,所以p1<p2,故D错误;
故选A.
点评:本题考查温度、压强对化学平衡移动影响,明确可逆反应特点结合“议一定二”原则分析解答,题目难度不大.

练习册系列答案
相关题目
下列命名错误的是( )
| A、4-乙基-3-戊醇 |
| B、2-甲基-1-丁醇 |
| C、2-甲基-1-丙醇 |
| D、4-甲基-2-己醇 |
硫酸镁和硫酸铝溶液等体积混合后,Al3+浓度为0.1mol?L-1,SO42-浓度为0.3mol?L-1,则混合液中镁离了的浓度为( )
| A、0.45mol?L-1 |
| B、0.3mol?L-1 |
| C、0.15mol?L-1 |
| D、0.1mol?L-1 |
下列实验操作中,正确的是( )
| A、蒸发溶液时,边加热加搅拌,直至蒸发皿内的液体蒸干 |
| B、量取25.00LKMnO4溶液时,应选择酸式滴定管 |
| C、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4注入容量瓶中加水稀释,边注入边搅拌 |
| D、配制一定物质的量浓度的溶液时,若未洗涤烧杯和玻璃棒,则会导致所配溶液的物质的量浓度偏高 |
下列化学用语正确的是( )
A、
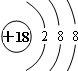 | ||||
B、HCl的电子式 | ||||
C、质量数为37的氯原子
| ||||
D、CH4分子的比例模型 |
下列有关实验装置的说法中正确的是( )
A、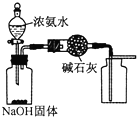 可制取干燥纯净的NH3 |
B、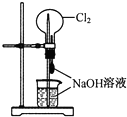 可以完成“喷泉”实验 |
C、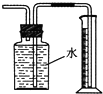 可测量Cu 与浓硝酸反应产生气体的体积 |
D、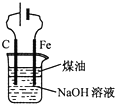 可用于实验室制备Fe (OH)2 |
能正确表示下列反应的离子方程式的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- |
| B、电解饱和食盐水:2Cl-+H2O═2OH-+H2↑+Cl2↑ |
| C、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| D、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
向含n mol 硫酸铝的溶液中加入m mol NaOH溶液,观察到的现象是先有白色沉淀生成,后部分溶解,则生成Al(OH)3沉淀的物质的量是( )
| A、(8n-m)mol |
| B、(4m-n)mol |
| C、(4n-m)mol |
| D、(7n-m)mol |
从葡萄籽中提取的原花青素结构为:有关原花青素的下列说法不正确的是( )
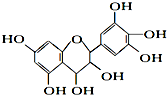

| A、该物质既可看作醇类,也可看作酚类 |
| B、1mol该物质可与4mol Br2反应 |
| C、1mol该物质可与7mol Na反应 |
| D、1mol该物质可与7mol NaOH反应 |