题目内容
2.下列说法正确的是( )| A. | CS2是极性键构成的极性分子 | |
| B. | SO2与CO2为等电子体 | |
| C. | 金属晶体的六方最密堆积和面心立方最密堆积的方式空间利用率最高 | |
| D. | 1molNaHSO4熔融态时有3mol离子 |
分析 A.分子结构对称,正负电荷中心重叠的分子属于非极性分子;
B.原子总数相同、电子总数或价电子总数相同的互为等电子体;
C.六方最密堆积和面心立方最密堆积空间利用率均为74%;
D.NaHSO4熔融态时电离出钠离子和硫酸氢根离子.
解答 解:A.CS2中C与S之间形成极性键,分子构型为直线型,分子结构对称,正负电荷中心重叠,属于非极性分子,故A错误;
B.SO2与CO2的原子数相同,电子数和价电子数都不同,所以不是等电子体,故B错误;
C.简单立方堆积空间利用率为52%,体心立方堆积空间利用率68%,六方最密堆积和面心立方最密堆积空间利用率均为74%,所以金属晶体的六方最密堆积和面心立方最密堆积的方式空间利用率最高,故C正确;
D.NaHSO4熔融态时电离出钠离子和硫酸氢根离子,所以1molNaHSO4熔融态时有2mol离子,故D错误.
故选C.
点评 本题考查了等电子体、分子极性和共价键的极性的判断、晶体的堆积方式、电解质的电离,明确等电子体的概念以及电子的计算、分子极性的判断等是解本题关键,题目难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
18.短周期主族元素X、Y、Z、W、Q的原子序数依次增大.X的最低负价与最高正价的代数和为0,Y原子和Z原子的最外层电子数均是其内层电子总数的$\frac{1}{2}$,下列说法正确的是( )
| A. | X的简单阴离子与Y的简单阳离子半径:X<Y | |
| B. | X分别与Z、W、Q形成的最简单化合物的稳定性:Z<W<Q | |
| C. | ZQ3分子中的所有原子最外层均满足8电子结构 | |
| D. | W、Q形成的含氧酸均为强酸. |
13.有4种碳架如下的烃,下列说法不正确的是( )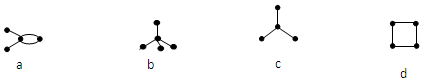
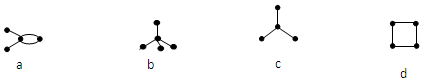
| A. | a和d是同分异构体 | B. | b和c是同系物 | ||
| C. | a和d都能发生加成反应 | D. | 只有a能使使酸性KMnO4溶液褪色 |
17.Cl和Cl-的相同之处是( )
| A. | 质子数 | B. | 核外电子数 | C. | 化学性质 | D. | 颜色 |
7.下列化学用语和叙述正确的是( )
| A. | Ca2+的结构示意图为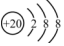 ,NH4Cl的电子式为 ,NH4Cl的电子式为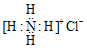 | |
| B. | 抗冰雪灾害时使用的融雪剂所含的氯化钠、氯化镁、氯化钙都属于盐 | |
| C. | 表示乙炔(CH≡CH)“燃烧热”的热化学方程式:CH≡CH(g)+$\frac{5}{2}{O_2}$(g)→2CO2(g)+H2O(g)+1256kJ | |
| D. | 质量数为16的氧原子:816O |
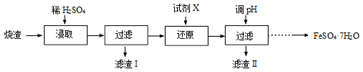
14.不同镜子背后的金属镀层可能是不同的,目前使用的金属主要有两种.为研究金属镀层的成分,某小组分别收集了两块镜子背面的金属镀层粉末甲和乙,按下述实验操作步骤进行实验:
根据实验,回答下列问题:
(1)甲与浓硝酸反应的化学方程式是Ag+2HNO3(浓)=AgNO3+NO2↑+H2O.
(2)实验操作⑤的实验现象是白色沉淀逐渐溶解至完全,乙溶解在NaOH溶液中反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)金属活动性:甲比乙弱.(填“强”、“弱”)
| 金属 | 实验操作 | 实验现象 |
| 甲 | ①取少量粉末,加入过量浓硝酸 ②向上述溶液中加入几滴NaCl溶液 | 粉末溶解,有红棕色气体产生 有白色沉淀生成 |
| 乙 | ③取少量粉末,加入足量NaOH溶液 ④向上述溶液中逐滴加入稀盐酸 ⑤继续加入过量的稀盐酸 | 粉末溶解,有气泡产生 有白色沉淀生成 白色沉淀溶解 |
(1)甲与浓硝酸反应的化学方程式是Ag+2HNO3(浓)=AgNO3+NO2↑+H2O.
(2)实验操作⑤的实验现象是白色沉淀逐渐溶解至完全,乙溶解在NaOH溶液中反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)金属活动性:甲比乙弱.(填“强”、“弱”)
11.下列说法错误的是( )
| A. | 淀粉和纤维素水解的最终产物都是葡萄糖 | |
| B. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| C. | 在加热或重金属盐的情况下,蛋白质都可发生变性 | |
| D. | 液化石油气和天然气的主要成分都是甲烷 |