题目内容
实验甲:3% H2O2直接分解;实验乙:3%H2O2中加入MnO2;现象,甲无明显现象;乙有大量气泡并试管发热.下列说法不正确的是( )
| A、该反应属于分解反应,且是放热反应 |
| B、MnO2是该反应的催化剂,且能改变该反应的反应热 |
| C、催化剂对反应速率有影响,对化学平衡无影响 |
| D、该反应是自发反应 |
考点:反应热和焓变,化学反应速率的影响因素
专题:化学反应中的能量变化
分析:A、H2O2分解为水和氧气,属于放热反应;
B、催化剂不能改变反应的反应热;
C、催化剂同等程度的改变正、逆化学反应速率;
D、在特定条件下,不需要外力进行的化学反应属于自发反应.
B、催化剂不能改变反应的反应热;
C、催化剂同等程度的改变正、逆化学反应速率;
D、在特定条件下,不需要外力进行的化学反应属于自发反应.
解答:
解:A、H2O2分解为水和氧气,属于放热反应,故A正确;
B、MnO2是该反应的催化剂,能改变反应的速率,不能改变反应的反应热,故B错误;
C、催化剂同等程度的改变正、逆化学反应速率,因此不影响化学平衡,故C正确;
D、在MnO2的催化作用下,H2O2自发分解为水和氧气,属于自发反应,故D正确;
故选B.
B、MnO2是该反应的催化剂,能改变反应的速率,不能改变反应的反应热,故B错误;
C、催化剂同等程度的改变正、逆化学反应速率,因此不影响化学平衡,故C正确;
D、在MnO2的催化作用下,H2O2自发分解为水和氧气,属于自发反应,故D正确;
故选B.
点评:本题考查了过氧化氢的分解反应实验,侧重于催化剂的反应热和催化剂的作用的考查,题目难度一般,注意催化剂同等程度的改变正、逆化学反应速率,不影响化学平衡、反应热.

练习册系列答案
相关题目
氰化钠(Na
N)是工业上冶炼黄金的重要原料,工业上生产氰化钠的化学方程式为2Na+2C+2NH3=2NaCN+3H2↑该反应中的还原剂为( )
| +2 |
| C |
| A、NH3 |
| B、C和Na |
| C、Na和NH3 |
| D、C和NH3 |
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是C( )
| A、Na+、K+、OH-、Cl- |
| B、Na+、Cu2+、SO42-、NO3- |
| C、Mg2+、Na+、SO42-、Cl- |
| D、Ba2+、Cl-、NO3-、K+ |
下列各组离子在溶液能大量共存,加入Fe2(SO4)3后仍能大量共存的是( )
| A、Na+I- CO32- ClO- |
| B、Fe2+ H+K+NO3- |
| C、Cu2+ Fe2+ Cl- NO3- |
| D、Ba2+Na+ SCN- Cl- |
某温下,重水(D2O)的离子积为1.6×10-15,若用pH一样地定义pD,则该温下关于pD叙述正确的是( )
| A、纯重水中pD=7 |
| B、1L溶有0.01molNaOD的D2O溶液中,溶液的pD=12 |
| C、1L溶有0.01molDCl的D2O溶液中,溶液的pD=2 |
| D、在100mL0.25mol/LNaOD的重水中,加入50mL0.2mol/L的DCl的重水溶液,其pD=1 |
在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g)?2c(g)△H<0,x(g)+3y(g)?2z(g)△H>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述正确的是( )
| A、恒容时,通入x气体,y的物质的量浓度增大 |
| B、恒容时,通入x气体,反应器中温度升高 |
| C、恒容时,通入惰性气体,各反应速率不变 |
| D、恒压时,通入惰性气体,c的物质的量不变 |
下列有关化学用语表示正确的是( )
A、比列模型 可以表示二氧化硫分子,也可以表示二氧化碳分子 可以表示二氧化硫分子,也可以表示二氧化碳分子 |
B、电子式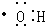 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
C、离子结构示意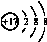 可以表示36Cl-,也可以表示37Cl- 可以表示36Cl-,也可以表示37Cl- |
| D、D结构简式(CH3)2CHOH可以表示1-丙醇,也可以表示2-丙醇 |