题目内容
将0.05 mol·L-1的HCl溶液和未知浓度的NaOH溶液以1∶2的体积比混合,所得混合液的pH为12.上述NaOH溶液12.5 mL与pH为3的某一元弱酸溶液20 mL恰好完全反应.试求:
(1)NaOH溶液的物质的量浓度.
(2)此一元弱酸的物质的量浓度.
答案:
解析:
解析:
|
答案:(1)c(NaOH)=0.04 mol·L-1;(2)一元弱酸的物质的量浓度为0.025 mol·L-1. 解析:设未知浓度的c(NaOH)=x, 则(2x-1 L×0.05 mol·L-1)÷3=0.01 mol·L-1,x=0.04 mol·L-1. 设一元弱酸的物质的量浓度为y, 0.04 mol·L-1×12.5×10-3 L=20×10-3 L·y,y=0.025 mol·L-1. |

练习册系列答案
相关题目
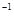 的盐酸与未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的PH为2。用上述 NaOH溶液与某一元弱酸HA 20.0mL反应,恰好中和时消耗NaOH溶液10.0mL,所得溶液PH为10。求:
的盐酸与未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的PH为2。用上述 NaOH溶液与某一元弱酸HA 20.0mL反应,恰好中和时消耗NaOH溶液10.0mL,所得溶液PH为10。求: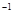 的盐酸与未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的PH为2。用上述 NaOH溶液与某一元弱酸HA 20.0mL反应,恰好中和时消耗NaOH溶液10.0mL,所得溶液PH为10。求:
的盐酸与未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的PH为2。用上述 NaOH溶液与某一元弱酸HA 20.0mL反应,恰好中和时消耗NaOH溶液10.0mL,所得溶液PH为10。求: