题目内容
(6分) 5.3g Na2CO3 正好与20mL盐酸完全反应(Na2CO3+2HCl=2NaCl+CO2↑+H2O)。问这种盐酸的物质的量浓度c(HCl)=________________________产生的CO2在标准状况下的体积V(CO2)=_____________________
【答案】
5 mol/L 1.12 L (每空3分,单位不对,扣1分)
【解析】5.3g碳酸钠的物质的量是5.3g÷106g/mol=0.05mol。根据方程式可知,消耗1mol碳酸钠的同时必然消耗2mol氯化氢,所以参加反应的氯化氢的物质的量是0.05mol×2=0.1mol,因此元素的浓度是0.1mol÷0.02L=5mol/L。生成CO2的物质的量是0.05mol,标准状况下的体积是0.05mol×22.4L/mol=1.12L。

练习册系列答案
相关题目
实验室欲配制480mL浓度为0.1mol?L-1的Na2CO3溶液,下列操作可以实现的是( )
| A、称量5.3g Na2CO3固体溶于480mL水配制成溶液 | B、称量5.3g Na2CO3固体溶于水配制成0.5L溶液 | C、称量5.3g Na2CO3?10H2O晶体溶于水配制成0.5L溶液 | D、称量5.3g Na2CO3?10H2O晶体溶于0.5L水配制成溶液 |
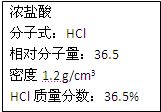 右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: