题目内容
17.在一定条件下,容积为2L的密闭容器中,将2mol M气体和3mol N气体混合,发生下列反应:2M(g)+3N(g)?xQ(g)+3R(g),该反应达到平衡时生成2.4mol R,并测得Q浓度 为0.4mol•L-1,下列叙述正确的是( )| A. | X值为2 | B. | 容器内压强不变 | ||
| C. | 平衡时N的浓度为0.6mol/L | D. | M的转化率为80% |
分析 该反应达到平衡时生成2.4mol R,并测得Q浓度 为0.4mol•L-1,则生成Q为0.4mol/L×2=0.8mol,则$\frac{x}{3}$=$\frac{0.8}{2.4}$,解得x=1,
2M(g)+3N(g)?Q(g)+3R(g)
开始 2 3 0 0
转化 1.6 2.4 0.8 2.4
平衡 0.4 0.6 0.8 2.4
结合c=$\frac{n}{V}$、转化率=$\frac{转化的量}{开始的量}$×100%计算.
解答 解:该反应达到平衡时生成2.4mol R,并测得Q浓度 为0.4mol•L-1,则生成Q为0.4mol/L×2=0.8mol,则$\frac{x}{3}$=$\frac{0.8}{2.4}$,解得x=1,
2M(g)+3N(g)?Q(g)+3R(g)
开始 2 3 0 0
转化 1.6 2.4 0.8 2.4
平衡 0.4 0.6 0.8 2.4
A.由上述计算可知,x=1,故A错误;
B.体积、温度不变,物质的量与压强成正比,该反应为气体物质的量减小的反应,则压强减小,故B错误;
C.平衡时N的浓度为$\frac{0.6mol}{2L}$=0.3mol/L,故C错误;
D.M的转化率为$\frac{1.6}{2}$×100%=80%,故D正确;
故选D.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、浓度及转化率的计算为解答的关键,侧重分析与计算能力的考查,注意x的确定方法,题目难度不大.

| A. | HCl溶于水能电离出H+、Cl-,所以HCl是离子化合物 | |
| B. | 碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 | |
| C. | He、CO2和CH4都是由分于构成,它们中都存在共价键 | |
| D. | NaHCO3受热分解生成Na2CO3、CO2和H2O,旣破坏了离子键,也破坏了共价键 |
| A. | CO的摩尔质量为28g | |
| B. | 32g O2含有的氧分子数为6.02×1023 | |
| C. | 标准状况下,22.4LC2H5OH的物质的量为1mol | |
| D. | 1mol•L-1NaCl溶液中含1mol Na+ |
| A. | A>B>D>C | B. | A>B>C>D | C. | C>D>A>B | D. | C>A>B>D |

| A. | 任何化学反应都伴随能量的变化 | |
| B. | 化学反应中的能量变化主要是由化学键的变化引起的 | |
| C. | 化学反应中能量的变化都表现为热量的变化 | |
| D. | 由图示可知CO+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO2+H2的反应为放热反应 |
 ,下列有关该材料的说法不正确的是( )
,下列有关该材料的说法不正确的是( )| A. | 该材料是通过加聚反应得到的产物 | |
| B. | 该材料在一定条件下能发生水解反应 | |
| C. | 该材料的单体是 | |
| D. | 该材料分子的聚合度是n |
| A. | 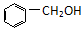 醇类-OH 醇类-OH | B. |  羧酸-COOH 羧酸-COOH | ||
| C. | 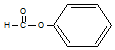 醛类-CHO 醛类-CHO | D. | CH3-O-CH3 醚类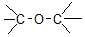 |
| A. | 氧化钙与水反应 | B. | 氮气液化 | C. | 碳酸钙分解 | D. | 浓硫酸稀释 |

 .
. $→_{△}^{O_{2}/Cu}$Y$→_{Ⅱ}^{一定条件}$乙
$→_{△}^{O_{2}/Cu}$Y$→_{Ⅱ}^{一定条件}$乙 ,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化.
,设计步骤Ⅰ的目的是保护碳碳双键,防止被氧化. .
. .
.