题目内容
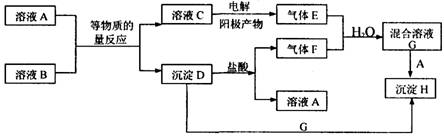
A、B均为无色盐溶液,B的焰色反应呈黄色,一定条件下A、B可以发生图所示的物质之间的一系列变化:

若E和F均为有刺激性气味的气体,H不溶于酸,请填写下列空白.
(1)气体E的化学式为 ,气体F的化学式为 ,C中溶质的化学式为 .
(2)写出下列反应的离子方程式:
C→E ;
D+G→H ;
(3)在混合溶液G中滴入几滴石蕊溶液,可见现象为 ,原因是 .

若E和F均为有刺激性气味的气体,H不溶于酸,请填写下列空白.
(1)气体E的化学式为
(2)写出下列反应的离子方程式:
C→E
D+G→H
(3)在混合溶液G中滴入几滴石蕊溶液,可见现象为
分析:A、B均为无色盐溶液,B的焰色反应呈黄色,判断B中含有钠元素,若E和F均为有刺激性气味的气体,E是电解溶液C得到的,分析判断C为含钠的化合物,H不溶于酸,沉淀D和G反应实现沉淀转化,推断H为硫酸钡沉淀,D为亚硫酸钡沉淀,E为黄绿色气体Cl2,F为无色刺激性气味的气体,并且能与E反应,应为SO2,则G应为硫酸和盐酸的混合物,H为BaSO4,A为BaCl2,D为BaSO3,B为Na2SO3,C为NaCl,结合对应物质的性质以及题目的要求可解答该题.
解答:解:A、B均为无色盐溶液,B的焰色反应呈黄色,判断B中含有钠元素,若E和F均为有刺激性气味的气体,E是电解溶液C得到的,分析判断C为含钠的化合物,H不溶于酸,沉淀D和G反应实现沉淀转化,推断H为硫酸钡沉淀,D为亚硫酸钡沉淀,E为黄绿色气体Cl2,F为无色刺激性气味的气体,并且能与E反应,应为SO2,则G应为硫酸和盐酸的混合物,H为BaSO4,A为BaCl2,D为BaSO3,B为Na2SO3,C为NaCl,
(1)由以上分析可知E为Cl2,F为SO2,C为NaCl,故答案为:Cl2;SO2;NaCl;
(2)C→E的反应为电解饱和食盐水的反应,方程式为2Cl-+2H2O
Cl2↑+H2↑+2OH-,D+G→H的反应为亚硫酸钡和混酸的反应,
反应的离子方程式为BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O;
(3)A为BaCl2,B为Na2SO3,因A与B是等物质的量混合发生反应Na2SO3+BaCl2=2NaCl+BaSO3↓,所以电解NaCl饱和溶液得到的Cl2和BaSO3与H2SO4反应生成的SO2亦为等物质的量,即Cl2与SO2恰好完全反应:SO2+Cl2+2H2O=2HCl+H2SO4,最终得到C溶液只有酸性而无漂白性,当二者等物质的量反应时生成盐酸和硫酸,溶液呈酸性,滴入几滴石蕊溶液,溶液变红,
故答案为:变红色;A为BaCl2,B为Na2SO3,因A与B是等物质的量混合发生反应Na2SO3+BaCl2=2NaCl+BaSO3↓,所以电解NaCl饱和溶液得到的Cl2和BaSO3与H2SO4反应生成的SO2亦为等物质的量,即Cl2与SO2恰好完全反应:SO2+Cl2+2H2O=2HCl+H2SO4,最终得到C溶液只有酸性而无漂白性.
(1)由以上分析可知E为Cl2,F为SO2,C为NaCl,故答案为:Cl2;SO2;NaCl;
(2)C→E的反应为电解饱和食盐水的反应,方程式为2Cl-+2H2O
| ||
反应的离子方程式为BaSO3+2H++SO42-=BaSO4↓+SO2↑+H2O,
故答案为:2Cl-+2H2O
| ||
(3)A为BaCl2,B为Na2SO3,因A与B是等物质的量混合发生反应Na2SO3+BaCl2=2NaCl+BaSO3↓,所以电解NaCl饱和溶液得到的Cl2和BaSO3与H2SO4反应生成的SO2亦为等物质的量,即Cl2与SO2恰好完全反应:SO2+Cl2+2H2O=2HCl+H2SO4,最终得到C溶液只有酸性而无漂白性,当二者等物质的量反应时生成盐酸和硫酸,溶液呈酸性,滴入几滴石蕊溶液,溶液变红,
故答案为:变红色;A为BaCl2,B为Na2SO3,因A与B是等物质的量混合发生反应Na2SO3+BaCl2=2NaCl+BaSO3↓,所以电解NaCl饱和溶液得到的Cl2和BaSO3与H2SO4反应生成的SO2亦为等物质的量,即Cl2与SO2恰好完全反应:SO2+Cl2+2H2O=2HCl+H2SO4,最终得到C溶液只有酸性而无漂白性.
点评:本题考查无机物的推断,本题注意以E、F的气味,沉淀特征和元素反应为推断该题的突破口,熟练掌握相关元素混合物的性质为解答该题的关键,该题很好地考查学生的思维、推断、分析能力,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


 : n(F)>1:1,则在混合溶液G中滴入几滴石蕊
: n(F)>1:1,则在混合溶液G中滴入几滴石蕊