题目内容
11.下列各分子中,所有原子最外层都满足8电子稳定结构的是( )| A. | XeF2 | B. | H2O | C. | CCl4 | D. | PCl5 |
分析 分子中某原子最外层电子数=元素原子最外层电子数+该元素原子化合价绝对值,若该值等于8,则该原子满足8电子结构,由此分析解答.
解答 解:A、二氟化氙中,Xe原子的原子核外最外层电子数为8,其在分子中的化合价为+2价,在分子中的原子最外层电子数为10,故A错误;
B、H2O分子中含有的共价键是极性共价键,且H原子不满足8电子稳定结构,故B错误;
C、CCl4分子中C原子最外层电子数是4,4+4=8,Cl原子最外层电子数是7,1+7=8,所以各原子最外层都满足8电子稳定结构,故C正确;
D、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故D错误.
故选C.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.下列说法不正确的是( )
| A. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| B. | 用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗盐酸的体积大 | |
| C. | 一定温度下,反应2Mg(S)+CO2(g)=2MgO(S)+C(s)能自发进行,则该反应△H<0 | |
| D. | 常温时,0.1mol•L-l CHCOOH 溶液加水稀释,$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$的值不变 |
19.化学与人类生活、生产和社会可持续发展密切相关,下列说法不正确的是( )
| A. | 为了给人类一个美好蓝天,化工企业推进脱硫、脱硝、除尘等设施改造,能大量减排SO2、NO2 | |
| B. | “PM2.5”是指大气中直径小于或等于2.5×10-6m的细小颗粒物,这些颗粒扩散在空气中形成胶体 | |
| C. | 实验场所严禁携带食物;禁止用饮料瓶装化学药品,防止误食 | |
| D. | 西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,双氧水、“84”消毒液均可以将病毒氧化而达到消毒的目的 |
16.工业上用某矿渣(含有Cu2O(主要)、Al2O3、Fe2O3、SiO2)提取铜的操作流程如图:
已知:Cu2O+2H+═Cu+Cu2++H2O
(1)固体混合物A中的成分是SiO2和Cu.
(2)反应Ⅰ完成后,铁元素的存在形式为Fe2+.(填离子符号)请写出生成该离子的离子方程式2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B可用于制造铁红,为了保证铁红的质量则x的取值为3.2≤X<4.0.
(4)书写出由沉淀C制备铝的化学方程式:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.

已知:Cu2O+2H+═Cu+Cu2++H2O
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
| 沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(2)反应Ⅰ完成后,铁元素的存在形式为Fe2+.(填离子符号)请写出生成该离子的离子方程式2Fe3++Cu=2Fe2++Cu2+.
(3)沉淀B可用于制造铁红,为了保证铁红的质量则x的取值为3.2≤X<4.0.
(4)书写出由沉淀C制备铝的化学方程式:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O、2Al2O3$\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑.
20.雷复尼特(结构是如图)是一种抗吸血虫病药,下列有关叙述不正确的是( )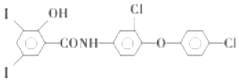

| A. | 与浓硫酸共热,有紫色气体产生 | B. | 分子中所有原子有可能在同一平面 | ||
| C. | 1mol只能与2molNaOH反应 | D. | 可使酸性高锰酸钾溶液褪色 |
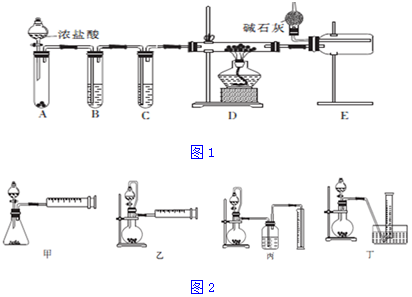
 有机物 A 是一种纯净的无色黏稠液体,易溶于水.为研究 A 的组成与结构,进行了如下实验,实验步骤:
有机物 A 是一种纯净的无色黏稠液体,易溶于水.为研究 A 的组成与结构,进行了如下实验,实验步骤: .
.
 与NaOH水溶液共热,生成的有机物的结构简式为
与NaOH水溶液共热,生成的有机物的结构简式为 .
. ;若该有机物有一个反式异构体,且能与氢气加成生成2-甲基戊烷,则该有机物的结构简式为
;若该有机物有一个反式异构体,且能与氢气加成生成2-甲基戊烷,则该有机物的结构简式为 .
.