题目内容
19.下列叙述中,正确的是( )| A. | 胶体属于介稳体系 | |
| B. | 蒸发操作中主要仪器是坩埚 | |
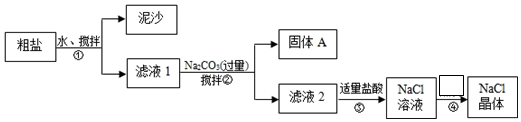
| C. | 粗盐经过溶解、过滤、蒸发后得到的是纯净的食盐 | |
| D. | NH4NO3不属于盐 |
分析 A.胶体的稳定性介于溶液与浊液之间,可发生聚沉;
B.在蒸发皿中进行蒸发操作;
C.粗盐经过溶解、过滤、蒸发后,只除去泥沙等不溶性杂质;
D.NH4NO3为铵根离子与硝酸根离子构成的盐.
解答 解:A.胶体的稳定性介于溶液与浊液之间,可发生聚沉,则胶体属于介稳体系,故A正确;
B.在蒸发皿中进行蒸发操作,而坩埚可用于结晶水的测定及物质加热分解实验,故B错误;
C.粗盐经过溶解、过滤、蒸发后,只除去泥沙等不溶性杂质,不能除去可溶性杂质,故C错误;
D.NH4NO3为铵根离子与硝酸根离子构成的盐,属于铵盐,故D错误;
故选A.
点评 本题考查较综合,涉及物质分类、混合物分离提纯,为高频考点,把握物质的组成、分类、性质及混合物分离提纯实验为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列物质的分类合理的是( )
| A. | 氧化物:CO2、NO、SO2、H2O | B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | ||
| C. | 铵盐:NH4Cl、NH4NO3、NH3•H2O | D. | 碱性氧化物:Na2O、CaO、CO2、Al2O3 |
7.在一密闭容器中,反应m A(g)+n B(g)?3C(g)达到平衡时,测得c(A)=0.5mol/L.在温度不变的情况下,将容积增大一倍,当达到新的平衡时,测得c(A)=0.3mol/L.下列判断中正确的是( )
| A. | A的质量分数增加 | B. | 平衡不移动 | ||
| C. | 化学计量数:m+n=3 | D. | 物质C的体积分数增大 |
14.下列防止金属腐蚀的做法不可行的是( )
| A. | 在铁制的炒锅、蒸锅等炊具上镀铜、防止生锈 | |
| B. | 地下钢铁管道连接镁块来防止钢铁锈蚀 | |
| C. | 健身器材刷油漆以防锈 | |
| D. | 洗衣机的滚筒采用不锈钢材料、既耐磨又耐腐蚀 |
4.浓度均为0.1mol•L-1的下列各组溶液,pH前者大于后者的是( )
| A. | NaH2PO4、Na2HPO4 | B. | Na2CO3、NaHCO3 | C. | NaHSO4、NaHCO3 | D. | Na2SO4、CH3COONa |
1.已知Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12.在只含有KCl、K2CrO4的混合溶液中滴加0.001mol•L-1的AgNO3溶液,当AgCl与Ag2CrO4共存时,测得溶液中CrO42-的浓度是5.000×10-3 mol•L-1,此时溶液中Cl-的物质的量浓度是( )
| A. | 1.36×10-5 mol•L-1 | B. | 8.90×10-6 mol•L-1 | ||
| C. | 4.45×10-2 mol•L-1 | D. | 1×10-5 mol•L-1 |
2.农业对化肥的需求是合成氨工业发展的持久推动力.
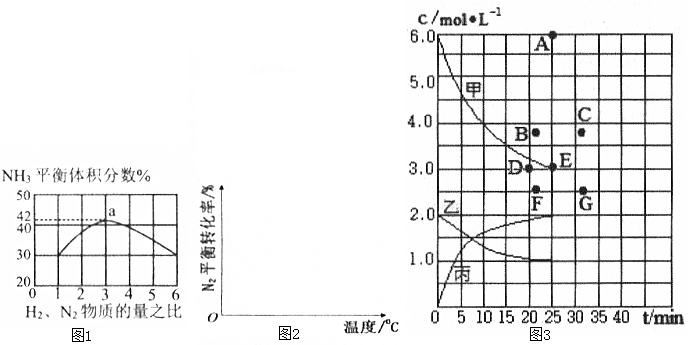
(1)已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.如图1表示500℃、60.0MPa条件下,原料气H2和N2的投料比与平衡时NH3体积分数的关系.
①工业上合成氨的温度一般控制在500℃,原因是该温度下催化剂的活性最好.
②根据图1中a点数据计算N2的平衡体积分数为14.5%,此时H2和N2的转化率之比为1:1.
(2)合成氨工业中,在其他条件相同时,请你画出N2的平衡转化率在不同压强(p1>p2)下随温度变化的曲线图.
(3)在500℃,反应N2(g)+3H2(g)?2NH3(g)中,将2mol N2和6mol H2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如表所示.
①根据上表实验数据,计算该反应的平衡常数K=$\frac{4}{27}$.(保留3位有效数字)
②该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度均为3mol/L,此时v正大于v逆(填“大于”、“小于”或“等于”).
③根据上表中数据得到的“浓度-时间”关系可用如图3中曲线表示,其中表示c(N2)-t的曲线是乙(填“甲”、“乙”或“丙”).在此温度下,若起始充入4molN2和12mol H2,反应刚达到平衡时,氢气的浓度可用B点表示(从A~G点中选择).
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(I)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.(已知:2H2(g)+O2(g)=2H2O(I)△H=-571.6kJ•mol-1)

(1)已知:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.如图1表示500℃、60.0MPa条件下,原料气H2和N2的投料比与平衡时NH3体积分数的关系.
①工业上合成氨的温度一般控制在500℃,原因是该温度下催化剂的活性最好.
②根据图1中a点数据计算N2的平衡体积分数为14.5%,此时H2和N2的转化率之比为1:1.
(2)合成氨工业中,在其他条件相同时,请你画出N2的平衡转化率在不同压强(p1>p2)下随温度变化的曲线图.

(3)在500℃,反应N2(g)+3H2(g)?2NH3(g)中,将2mol N2和6mol H2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如表所示.
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| N(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| N(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
②该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度均为3mol/L,此时v正大于v逆(填“大于”、“小于”或“等于”).
③根据上表中数据得到的“浓度-时间”关系可用如图3中曲线表示,其中表示c(N2)-t的曲线是乙(填“甲”、“乙”或“丙”).在此温度下,若起始充入4molN2和12mol H2,反应刚达到平衡时,氢气的浓度可用B点表示(从A~G点中选择).
(4)近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(I)?4NH3(g)+3O2(g),则其反应热△H=+1530 kJ•mol-1.(已知:2H2(g)+O2(g)=2H2O(I)△H=-571.6kJ•mol-1)