题目内容
防止水体污染,改善水质,最根本的措施是控制工业废水和生活污水的排放.有一种工业废水,已知其中含有大量的Fe2+ 和SO42-,少量的Ag+和Na+,以及部分污泥.某校化学兴趣小组同学通过下列操作过程,回收物质,处理废水.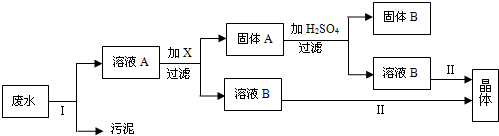
根据上述操作过程,回答下列问题:
(1)在实验室进行Ⅰ操作时,需要的主要玻璃仪器有______.
(2)操作Ⅱ的名称是______.
(3)向溶液A中需要加入过量X,X是______,发生反应的离子方程式为______.
(4)上述操作回收到的物质B是______,晶体是______.(两空均写名称)
解:废水经过滤后可得含有大量的Fe2+ 和SO42-,少量的Ag+和Na+的溶液,然后在滤液中加入过量Fe可置换出Ag,则固体A为Ag和Fe的混合物,加入硫酸可得硫酸亚铁溶液,固体B为Ag,则
(1)Ⅰ操作为过滤,需要的玻璃仪器有漏斗、烧杯、玻璃棒,故答案为:漏斗、烧杯、玻璃棒;
(2)溶液B为硫酸亚铁溶液,要得到硫酸亚铁晶体,应进行蒸发结晶操作,故答案为:蒸发结晶;
(3)由以上分析可知X为Fe,发生反应为Fe+2Ag+=Fe2++2Ag,可置换出Ag,进而回收,
故答案为:Fe;Fe+2Ag+=Fe2++2Ag;
(4)固体B为Ag,溶液B为硫酸亚铁,可得到硫酸亚铁晶体,故答案为:银;硫酸亚铁晶体.
分析:废水经过滤后可得含有大量的Fe2+ 和SO42-,少量的Ag+和Na+的溶液,然后在滤液中加入过量Fe可置换出Ag,则固体A为Ag和Fe的混合物,加入硫酸可得硫酸亚铁溶液,固体B为Ag,以此解答该题.
点评:本题考查物质的分离、提出操作,题目难度不大,注意把握物质的性质,结合分离流程可解答该题.答题时注意体会做题思路.
(1)Ⅰ操作为过滤,需要的玻璃仪器有漏斗、烧杯、玻璃棒,故答案为:漏斗、烧杯、玻璃棒;
(2)溶液B为硫酸亚铁溶液,要得到硫酸亚铁晶体,应进行蒸发结晶操作,故答案为:蒸发结晶;
(3)由以上分析可知X为Fe,发生反应为Fe+2Ag+=Fe2++2Ag,可置换出Ag,进而回收,
故答案为:Fe;Fe+2Ag+=Fe2++2Ag;
(4)固体B为Ag,溶液B为硫酸亚铁,可得到硫酸亚铁晶体,故答案为:银;硫酸亚铁晶体.
分析:废水经过滤后可得含有大量的Fe2+ 和SO42-,少量的Ag+和Na+的溶液,然后在滤液中加入过量Fe可置换出Ag,则固体A为Ag和Fe的混合物,加入硫酸可得硫酸亚铁溶液,固体B为Ag,以此解答该题.
点评:本题考查物质的分离、提出操作,题目难度不大,注意把握物质的性质,结合分离流程可解答该题.答题时注意体会做题思路.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
《化学与生活》
(1)现有下列几种物质 A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素F.阿司匹林。请按下列要求填空(填序号)。
富含维生素C的是 ;应用最广泛的抗生素之一的是 ;可直接进入血液补充能量的是 ;食用过多会引起血压升高、肾脏受损的是 。
(2)人体摄入的蛋白质,在酶的催化作用下发生水解,最终生成氨基酸。这些氨基酸一部分重新合成人体所需的蛋白质、糖或脂类物质,以满足各种生命活动的需要;另一部分则发生氧化反应,释放能量。
①蛋白质分子中主要含有 四种元素。
②蛋白质溶液遇到浓的硫酸铵等无机盐溶液,会析出沉淀;再加适量水后,蛋白质重新溶解,仍然具有原来的活性。这个过程称为 。
③人体中共有二十多种氨基酸,其中有几种是人体自身不能合成的,必须由食物获得,称为 氨基酸。
(3)防止水体污染,改善水质,最根本的措施是控制工业废水和生活污水的排放。有一种工业废水,已知其中含有大量的Fe2+ 和SO42-,少量的Ag+和Na+,以及部分污泥。某校化学兴趣小组同学通过下列操作过程,回收物质,处理废水。


根据上述操作过程,回答下列问题:
|
|
b.操作②的名称是 。
c.向溶液A中需要加入过量X,X是 ,发生反应的离子方程式为 。
d.上述操作回收到的物质是 。