题目内容
18.某有机化合物的结构简式为: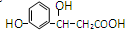 ,它可以发生反应的类型有①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚,其中组合完全且正确的是( )
,它可以发生反应的类型有①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚,其中组合完全且正确的是( )| A. | ①②③④ | B. | ①②④⑤ | C. | ①②⑤⑥ | D. | ①②③④⑤ |
分析 分子中含酚-OH、醇-OH、-COOH,结合酚、醇、羧酸的性质来解答.
解答 解:含酚-OH,可发生氧化、取代反应;
含醇-OH,额发生消去、酯化反应、氧化反应;
含苯环可发生加成反应;
含-OH、-COOH可发生缩聚反应;
不能发生水解、加聚反应,
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸、醇的性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
8.镁燃料电池具有比能量(指参与电极反应的单位质量的电极材料放出电能的大小)高、燃料易于贮运等优点,拥有良好的应用前景,下图为“镁-次氯酸盐”燃料电池原理示意图,总反应为Mg+ClO-+H2O═Mg(OH)2+Cl-,镁合金电极可以是Mg与Al或Li的合金.下列说法不正确的( )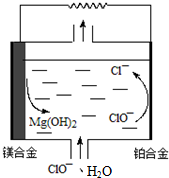

| A. | Mg-Li合金比传统的Mg-Al合金具有更高的比能量 | |
| B. | 铂合金的电极反应:ClO-+H2O═Cl-+2OH--2e-,OH-向镁合金电极迁移 | |
| C. | 该电池镁合金会发生自身腐蚀产生氢气,使电极利用率降低 | |
| D. | 把电解质换成H2O2、H2SO4和NaCl的混合溶液,工作时H2O2将参与电极反应,其电极反应为:2H2O2-2e-═O2↑+2H2O |
9.类推的思维方法可解决不少化学问题,但类推的结论最终要经过实践的检验才能确定其正确与否.下列几种类推结论中,你认为正确的是( )
| A. | 沸点HBr>HCl,则同族元素氢化物沸点HCl>HF | |
| B. | Fe3O4可表示为FeO•Fe2O3,则Pb3O4可表示为PbO•Pb2O3 | |
| C. | CO2与Na2O2反应只生成Na2CO3和O2,故SO2与Na2O2反应也只生成Na2SO3和O2 | |
| D. | 因为N元素的非金属性比P元素强,所以HNO3的酸性强于H3PO4 |
6.化学反应处于平衡状态时,下列说法正确的是( )
| A. | 反应不再进行 | B. | 反应物浓度等于生成物浓度 | ||
| C. | 正反应速率不等于逆反应速率 | D. | 各组分浓度不再随时间而变化 |
3.下列说法错误的是( )
| A. | 胶体粒子能透过滤纸,但不能透过半透膜 | |
| B. | 胶体和溶液的本质区别在于分散质粒子大小 | |
| C. | 蛋清、豆浆、墨水都是胶体 | |
| D. | 丁达尔效应是化学变化 |
10.设NA为阿伏加罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 3mol铁与足量的水蒸气充分反应,转移8NA个电子 | |
| C. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA | |
| D. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
7.原电池中,B极逐渐变粗,A极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
| A. | A是Zn,B是Cu,C为稀硫酸 | B. | A是Cu,B是Zn,C为稀硫酸 | ||
| C. | A是Fe,B是Ag,C为稀AgNO3溶液 | D. | A是Ag,B是Fe,C为稀AgNO3溶液 |
8.下列金属防腐的措施中,属于牺牲阳极的阴极保护法的是( )
| A. | 水中的钢闸门连接电源的负极 | |
| B. | 地下钢管连接锌板 | |
| C. | 铁件镀铜 | |
| D. | 自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨 |