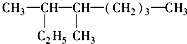题目内容
在实验室里,李真棒同学要做证明Cl、Br、I的非金属性依次减弱的实验,所需试剂除NaCl溶液、NaBr溶液、KI溶液外,还需要的试剂为 ,证明Cl、I非金属性强弱的离子方程式为 .
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:实验设计题
分析:活动性强的非金属单质能将活动性弱的非金属置换出来,可以选择氯气,用氯气和碘离子反应,证明Cl、I非金属性强弱.
解答:
解:由Cl2+2NaI=2NaCl+I2,说明非金属单质的活动性Cl2>I2;Cl2+2NaBr=2NaCl+Br2,说明非金属单质的活动性Cl2>Br2,生成的溴还可以与KI溶液反应,综合上述分析可知,其活动性由强到弱的顺序为Cl2>Br2>I2,证明Cl、I非金属性强弱的离子方程式为Cl2+2I-=2Cl-+I2,
故答案为:过量的氯气;Cl2+2I-=2Cl-+I2.
故答案为:过量的氯气;Cl2+2I-=2Cl-+I2.
点评:本题考查了非金属单质活动性的判断,完成此题,可以依据金属活动性的意义以及题干提供的信息进行.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
常温下,把一定体积、浓度的氨水滴加到一定体积、浓度的盐酸中和后,溶液中C(NH4+)=C(Cl-),则中和后溶液的pH( )
| A、等于7 | B、大于7 |
| C、小于7 | D、无法确定 |
H2O2只做还原剂的反应是( )
| A、H2O2+2KI═2KOH+I2 |
| B、4H2O2+PbS═PbSO4+4H2O |
| C、2H2O2═2 H2O+O2↑ |
| D、2H2O2+Cl2=2HCl+O2↑ |
下列说法中正确的是( )
| A、可逆反应的特征是反应物和生成物的浓度相等 |
| B、在其他条件不变时,升高温度可以使化学平衡向放热反应的方向移动 |
| C、在其他条件不变时,使用催化剂可以改变化学反应速率,但不能改变化学平衡状态 |
| D、在其他条件不变时,增大压强一定会破坏有气体存在的反应的平衡状态 |
下列物质的类别与所含官能团都正确的是( )
A、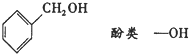 |
B、 |
C、 |
D、 |