题目内容
14.影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过图(1)所示装置研究反应速率的有关问题.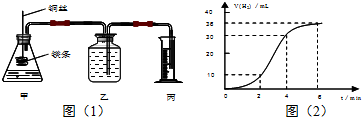
(1)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中.镁条与足量盐酸反应生成H2的量与反应时间的关系曲线如图(2)所示.
①请在答卷方框中画出上述反应的速率(mL/min)与时间(min)的关系曲线.
②在前4min内,镁条与盐酸的反应速率逐渐加快,在4min之后,反应速率逐渐减慢,请简述其原因:镁和盐酸反应是放热反应,随着反应体系温度升高,反应速率增大;4min后由于溶液中H+浓度降低,所以导致反应速率减小.
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快.他决定对其原因进行探究.填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO42-对反应没有影响;
原因Ⅱ:Cl-对反应没有影响,而SO42-对反应具有阻碍作用;
原因Ⅲ:Cl-对反应具有促进作用,而SO42-对反应具有阻碍作用;
原因Ⅳ:Cl-、SO42-均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:Cl-、SO42-均对反应具有阻碍作用,但Cl-影响更小(或SO42-影响更大).
②该同学设计并进行了两组实验,即得出了正确结论.他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化.
若观察到实验a中反应速率加快,实验b中反应速率减慢,则说明原因Ⅲ是正确的.依此类推.该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用.
分析 (1)①先根据图2找出2、4、6min时刻时的氢气体积的变化量,再找出2、4、6min时刻时的速率与时间的关系,然后用平滑曲线描绘图象;
②根据该反应的反应热及溶液中氢离子的浓度判断;
(2)①原因Ⅱ:先确定Cl-对反应没有影响再猜测硫酸根离子的作用;
原因Ⅴ:根据原因Ⅳ提出与原因Ⅳ相反的观点;
②根据a、b对比实验中的现象判断原因Ⅲ.
解答 解:(1)①2、4、6min时刻时氢气体积的分别为10 mL、20mL、36mL,其平均反应速率分别为5 mL/min、7.5mL/min、6mL/min,然后标出速率与时间图象为: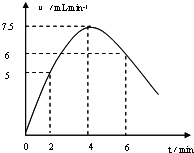 ,
,
故答案为: ;
;
②该反应是放热反应,随着反应的进行,放出的热量越多,溶液的温度越高,反应速率越大;随着反应的进行,溶液中氢离子的浓度逐渐减小,浓度越小,反应速率越小.
故答案为:镁和盐酸反应是放热反应,随着反应体系温度升高,反应速率增大;4min后由于溶液中H+浓度降低,所以导致反应速率减小;
(2)①根据原因Ⅰ结合题意,提出与原因Ⅰ相反的观点,原因Ⅱ为:Cl-对反应没有影响,而SO42-对反应具有阻碍作用,
故答案为:Cl-对反应没有影响,而SO42-对反应具有阻碍作用;
根据原因Ⅳ结合题意,提出与原因Ⅳ相反的观点,原因Ⅴ为:Cl-、SO42-均对反应具有阻碍作用,但Cl-影响更小(或SO42-影响更大),
故答案为:Cl-、SO42-均对反应具有阻碍作用,但Cl-影响更小(或SO42-影响更大).
②a中原来时快有硫酸根离子,后加入氯离子,如果氯离子有促进作用,那么反应速率就比未加时快,以此证明原因Ⅲ是正确的;
b中中原来时快有氯离子,后加入硫酸根离子,如果硫酸根离子有阻碍作用,那么反应速率比未加时慢,以此说明因Ⅲ是正确的,
故答案为:反应速率加快;反应速率减慢.
点评 本题考查了影响化学反应速率的因素,题目难度中等,影响化学反应速率的外界条件有:温度、浓度、压强、催化剂等,试题知识点较多、综合性较强,充分考查了学生得到分析能力及化学实验能力.

| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 四 | ⑧ | ⑨ |
(2)实验室制取②的氢化物的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(3)④和⑤元素最高价氧化物对应的水化物相互反应的化学方程式NaOH+Al(OH)3=NaAlO2+2H2O;
(4)元素②、⑥与氢元素形成的一种化合物含有的化学键类型有离子键、共价键;其电子式为
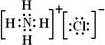 .
. I.(1)将硫化钠溶液与氯化铝溶液混合,有白色沉淀和气体生成,但此沉淀不是硫化铝.写出该反应的离子反应方程式:2Al3++3S2-+6H2O═2Al(OH)3↓+3H2S↑.
(2)将NH3通过灼热的CuO,有无色无味的难溶于水的气体生成,写出该反应的化学方程式:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O.
(3)CoCl2常用作多彩水泥的添加剂,可用钴的某种氧化物与盐酸反应制备(其中Co的化合价为+2、+3).现取适量这种钴的氧化物,可与480mL 5mol•L-1盐酸恰好完全反应,得到CoCl2溶液和6.72L黄绿色气体(标准状况).则该反应的化学反应方程式为Co3O4+8HCl═3CoCl2+Cl2↑+4H2O.
II.下表给出五种元素的相关信息,其中A、B、C、D为短周期元素.根据以下信息填空:
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
(5)化合物X是元素D的最高价氧化物的水化物,X在水中的电离方程为H2SO4═2H++SO42-;常温下,E的单质与化合物X稀溶液反应生成盐Y,Y的化学式是FeSO4.化合物Z仅由元素D和E组成,Z+H2O+O2→X+Y,产物中n(X):n(Y)=1:1,写出并配平上述方程式:2FeS2+2H2O+7O2═2FeSO4+2H2SO4.
(6)盐Y受强热会发生分解反应,其气体产物由元素D的氧化物组成,请设计一个可行的定性实验,验证其气体产物中所含元素D的氧化物的组成将气体产物通入品红溶液,如果品红溶液褪色,则含有SO2,反之则无SO2.取适量吸收液于试管,滴加适量盐酸酸化,再滴加BaCl2,如有白色沉淀生成,则含有SO3,反之则无SO3..
| A. | 氢氧化铝是白色胶状沉淀,能凝聚水中的悬浮物,但不能吸附色素 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大题水冲洗,然后涂上硼酸 | |
| C. | 氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 | |
| D. | 酒精灯着火时可用水扑灭 |
| A. | 有大量的氯气泄漏时,用肥皂水浸湿软布蒙面,并迅速离开现场 | |
| B. | 氢气在盛有氯气的集气瓶中燃烧,瓶口有白烟产生 | |
| C. | 氯气能与铁反应,液氯不宜贮存在钢瓶中 | |
| D. | 工业上以氯气和澄清石灰水为原料制造漂白粉 |
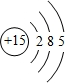 ,E的最高价含氧酸的化学式HClO4.
,E的最高价含氧酸的化学式HClO4.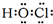 .
.
 已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O. X、Z、Q、R、T为前四周期元素,且原子序数依次增大.X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子.请回答下列问题:
X、Z、Q、R、T为前四周期元素,且原子序数依次增大.X和Q属同族元素,X和R可形成化合物XR4;R2为黄绿色气体;Z与X同周期且基态原子的s轨道和p轨道的电子总数相等;T2+的3d 轨道中有5个电子.请回答下列问题: