题目内容
20.下列实验操作或装置不符合实验要求的是( )| 选项 | A | B | C | D |
| 操作 | 从CCl4萃取溴水中溴后的混合液中分离 | 二氧化锰与浓盐酸反应制干燥氯气 | 可用于制备并观察氢氧化铁沉淀 | 检查装置气密性 |
| 实验装置 | 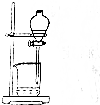 | 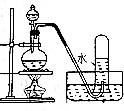 | 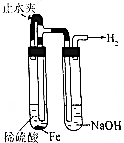 | 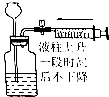 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.溴单质不溶于四氯化碳,可通过分液操作分离;
B.制取干燥氯气,不能使用排水法收集;
C.用氢气排出装置中空气,可以长时间观察氢氧化亚铁;
D.通过推动注射器,根据长颈漏斗下端形成的水柱情况可判断装置的气密性.
解答 解:A.溴单质原溶液四氯化碳,不溶于水,可通过分液操作分离,图示装置合理,故A正确;
B.通过排水法收集氯气,无法获得干燥氯气,故B错误;
C.铁与稀硫酸反应生成氢气,氢气将装置中空气排出,硫酸亚铁与氢氧化钠反应生成氢氧化亚铁,从而可长时间观察到氢氧化亚铁,能够达到实验目的,故C正确;
D.推动注射器,若长颈漏斗下端形成水柱,且一段时间内水柱不发生变化,则证明装置的气密性良好,故D正确;
故选B.
点评 本题考查了性质实验方案的设计与评价,题目难度中等,明确常见实验装置的特点及使用方法为解答关键,注意掌握性质实验方案的设计与评价方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
11.铬及其化合物在工业上有许多用途,但化工废料铬渣对人体健康有很大危害.
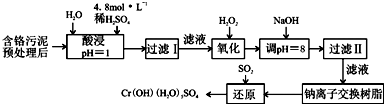
以制革工业产生的污泥为原料,回收污泥中三价铬的工艺流程如图所示,(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+):
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
(1)能提高酸浸时三价铬的浸取率的措施有ABC(填字母)
A.将含铬污泥粉碎并适当延长浸取时间 B.升高温度不断搅拌 C.多次浸取,合并浸取液 D.缩短浸取时间
(2)氧化过程中加入H2O2,除了能把Cr3+氧化为Cr2O72-外,另一个作用是2Fe2++2H++H2O2=2Fe3++2H2O(用离子方程式表示)
(3)过滤Ⅱ产生的沉淀是Fe(OH)3、Al(OH)3、Cu(OH)2,(填化学式)
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+,Mg2+(填离子符号)
(5)每生成1molCr(OH)(H2O)3SO4,消耗SO2的物质的量为1.5mol
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解,经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去
①铁电极与直流电源的正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)3]=6.0×10-31)
以制革工业产生的污泥为原料,回收污泥中三价铬的工艺流程如图所示,(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
A.将含铬污泥粉碎并适当延长浸取时间 B.升高温度不断搅拌 C.多次浸取,合并浸取液 D.缩短浸取时间
(2)氧化过程中加入H2O2,除了能把Cr3+氧化为Cr2O72-外,另一个作用是2Fe2++2H++H2O2=2Fe3++2H2O(用离子方程式表示)
(3)过滤Ⅱ产生的沉淀是Fe(OH)3、Al(OH)3、Cu(OH)2,(填化学式)
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+,Mg2+(填离子符号)
(5)每生成1molCr(OH)(H2O)3SO4,消耗SO2的物质的量为1.5mol
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解,经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去
①铁电极与直流电源的正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)3]=6.0×10-31)
8.下列关于有机物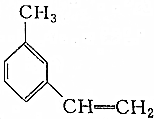 的命名正确的是( )
的命名正确的是( )
 的命名正确的是( )
的命名正确的是( )| A. | 1-甲基-3-乙基苯 | B. | 1-甲基-3-苯乙烯 | C. | 间甲基苯乙烯 | D. | 间乙基甲苯 |
2.如图1表示mA(g)+nB(g)?pC(g)+qD(g),在不同温度下经过一定时间混合体系中C的质量分数与温度T的关系;如图2表示在一定条件下达到平衡(v正=v逆)后t时刻改变影响平衡的一个条件重新建立新平衡的反应过程,判断该反应是( )


| A. | m+n<p+q△H>0 | B. | m+n>p+q△H>0 | C. | m+n<p+q△H<0 | D. | m+n>p+q△H<0 |
7.在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是( )
| A. | 制催化剂的材料 | B. | 耐高温、耐腐蚀的合金材料 | ||
| C. | 半导体材料 | D. | 制农药的材料 |
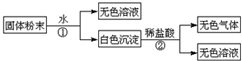
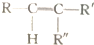 $\stackrel{高锰酸钾酸性溶液}{→}$R-COOH+
$\stackrel{高锰酸钾酸性溶液}{→}$R-COOH+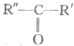
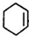 ,HOOC(CH2)4COOH.
,HOOC(CH2)4COOH.