题目内容
1.分类是学习化学的方法之一,下列各组物质按氧化物、酸、碱、盐顺序排列的一组是( )| A. | 氢氧化铁、硝酸、烧碱、氯化钠 | B. | 干冰、碳酸、纯碱、硫酸钾 | ||
| C. | 水、硫酸、熟石灰、氯化钾 | D. | 氨水、醋酸、氢氧化铁、食盐 |
分析 由两种元素构成、其中一种为氧元素的为氧化物;
电离出的阳离子全部是氢离子的化合物为酸;
电离出阴离子全部是氢氧根的化合物为碱;
阴离子是酸根离子、阳离子是金属离子或铵根离子的化合物为盐,据此分析.
解答 解:A、氢氧化铁是碱而不是氧化物,故A错误;
B、纯碱为碳酸钠,是盐不是碱,故B错误;
C、水是氧化物;硫酸是酸;熟石灰是氢氧化钙,是碱;氯化钾为盐,故C正确;
D、氨水是混合物,不是氧化物,故D错误.
故选C.
点评 本题考查了氧化物、酸、碱、盐的概念和辨别,难度不大,应注意基础的掌握.

练习册系列答案
相关题目
11. 某实验小组用如图装置制备家用消毒液,并探究其性质.
某实验小组用如图装置制备家用消毒液,并探究其性质.
反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
(1)写出利用上述装置制备消毒液涉及反应的化学方程式4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+MnCl2+2H2O、 Cl2+2NaOH═NaClO+NaCl+H2O.
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去为探究操作a中溶液褪色的原因,又补充了如下实验:
获得结论:此实验小组制备的消毒液具有漂白性性.
(3)该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降.
①操作b中溶液变成黄绿色的原因:2H++ClO-+Cl-═Cl2↑+H2O(用离子方程式表示).
②有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色.
(4)有效氯的含量是检测含氯消毒剂消毒效果的重要指标.具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上.小组同学进行如下实验测定有效氯:
取此消毒液5g,加入20mL 0.5mol•L-1KI溶液,10mL 2mol•L-1的硫酸溶液;加几滴淀粉溶液后,用0.1mol•L-1Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O320mL.(已知:2S2O32-+I2═S4O62-+2I-).注:相对原子质量Cl35.5,Na23,S32,O 16,I 127,K39
①达到滴定终点时的实验现象是溶液蓝色褪去且半分钟不恢复.
②此消毒液有效氯含量为1.42%(保留一位有效数字).
获得结论:此实验制得的消毒液不符合(填“符合”或“不符合”)家用要求.
 某实验小组用如图装置制备家用消毒液,并探究其性质.
某实验小组用如图装置制备家用消毒液,并探究其性质.反应停止后,取洗气瓶中无色溶液5mL分别进行了如下实验:
| 操作 | 现象 |
| a.测溶液pH,并向其中滴加2滴酚酞 | pH=13,溶液变红,5min后褪色 |
| b.向其中逐滴加入盐酸 | 溶液逐渐变成黄绿色 |
(2)查阅资料:酚酞的变色范围为8.2~10,且酚酞在强碱性溶液中红色会褪去为探究操作a中溶液褪色的原因,又补充了如下实验:
| 操作 | 现象 |
| 取5mLpH=13NaOH溶液,向其中滴加2滴酚酞 | 溶液变红,30min后褪色 |
(3)该小组由操作b获得结论:随着溶液酸性的增强,此消毒液的稳定性下降.
①操作b中溶液变成黄绿色的原因:2H++ClO-+Cl-═Cl2↑+H2O(用离子方程式表示).
②有同学认为由操作b获得上述结论并不严谨,需要进一步确认此结论的实验方案是取洗气瓶中溶液5mL,向其中逐滴加入硫酸,观察溶液是否逐渐变为黄绿色.
(4)有效氯的含量是检测含氯消毒剂消毒效果的重要指标.具体用“单位质量的含氯消毒液在酸性条件下所能释放出氯气的质量”进行表征,一般家用消毒液有效氯含量在5%以上.小组同学进行如下实验测定有效氯:
取此消毒液5g,加入20mL 0.5mol•L-1KI溶液,10mL 2mol•L-1的硫酸溶液;加几滴淀粉溶液后,用0.1mol•L-1Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O320mL.(已知:2S2O32-+I2═S4O62-+2I-).注:相对原子质量Cl35.5,Na23,S32,O 16,I 127,K39
①达到滴定终点时的实验现象是溶液蓝色褪去且半分钟不恢复.
②此消毒液有效氯含量为1.42%(保留一位有效数字).
获得结论:此实验制得的消毒液不符合(填“符合”或“不符合”)家用要求.
6.下列反应的热效应与其它三项不相同的是( )
| A. | 氯化铵与Ba(OH)2•8H2O反应 | B. | 钠与冷水反应 | ||
| C. | 锌片与稀硫酸反应 | D. | 铝粉与三氧化二铁的反应 |
10.原子序数依次增大的短周期主族元素X、Y、Z、W只位于2个主族,X与Z的核电荷数之和等于Y与W最外层电子数之和,4种元素中只有2种金属元素.下列说法正确的是( )
| A. | X属于非金属元素 | B. | 对应的氢化物的热稳定性:W>Y | ||
| C. | W与Z易于形成离子化合物 | D. | Z离子的氧化性强于X离子 |
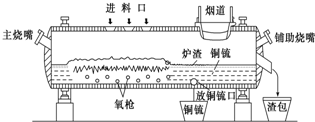
 随着工业发展和社会的进步,人们日益关注环境污染问题.
随着工业发展和社会的进步,人们日益关注环境污染问题.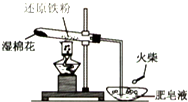 为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.
为探究铁和铁的化合物的一些化学性质,某学生实验小组设计了以下实验.