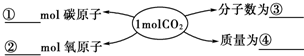
题目内容
某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O.已知K2S2O8的氧化性比K2Cr2O7强.
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(要求配平)
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 剂.
(3)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 .
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(要求配平)
(2)反应中,被还原的物质是
(3)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为
考点:氧化还原反应
专题:氧化还原反应专题
分析:K2S2O8的氧化性比K2Cr2O7强,则Cr2(SO4)3→K2Cr2O7铬元素化合价升高,K2S2O8→K2SO4、H2SO4硫元素化合价降低,所以反应物为K2S2O8和Cr2(SO4)3,生成物为K2Cr2O7、K2SO4、H2SO4,发生K2S2O8+Cr2(SO4)3+H2O→K2Cr2O7+K2SO4+H2SO4,以此来解答.
解答:
解:K2S2O8的氧化性比K2Cr2O7强,则Cr2(SO4)3→K2Cr2O7铬元素化合价升高,K2S2O8→K2SO4、H2SO4硫元素化合价降低,所以反应物为K2S2O8和Cr2(SO4)3,生成物为K2Cr2O7、K2SO4、H2SO4,发生K2S2O8+Cr2(SO4)3+H2O→K2Cr2O7+K2SO4+H2SO4,
(1)由电子守恒、原子守恒可知反应为7H2O+Cr2(SO4)3+3K2S2O8=7H2SO4+2K2SO4+K2Cr2O7,故答案为:7H2O+Cr2(SO4)3+3K2S2O8=7H2SO4+2K2SO4+K2Cr2O7;
(2)K2S2O8中S化合价降低,被还原;Cr2(SO4)3中Cr元素化合价升高被氧化,是还原剂,故答案为:K2S2O8;还原;
(3)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应,铬元素化合价由+6→+3,K2Cr2O7做氧化剂被还原,H2C2O4中的碳元素由+3→+4化合价升高被氧化,做还原剂,设还原剂的物质的物质的量x,氧化剂物质的量为y,由电子守恒规律可得x×2×(4-3)=y×2×(6-3),解得x:y=3:1,故答案为:3:1.
(1)由电子守恒、原子守恒可知反应为7H2O+Cr2(SO4)3+3K2S2O8=7H2SO4+2K2SO4+K2Cr2O7,故答案为:7H2O+Cr2(SO4)3+3K2S2O8=7H2SO4+2K2SO4+K2Cr2O7;
(2)K2S2O8中S化合价降低,被还原;Cr2(SO4)3中Cr元素化合价升高被氧化,是还原剂,故答案为:K2S2O8;还原;
(3)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应,铬元素化合价由+6→+3,K2Cr2O7做氧化剂被还原,H2C2O4中的碳元素由+3→+4化合价升高被氧化,做还原剂,设还原剂的物质的物质的量x,氧化剂物质的量为y,由电子守恒规律可得x×2×(4-3)=y×2×(6-3),解得x:y=3:1,故答案为:3:1.
点评:本题考查氧化还原反应及计算,为高频考点,把握发生的反应、反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及计算的考查,题目难度不大.

练习册系列答案
相关题目
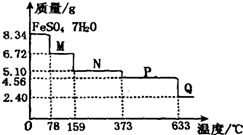 取8.34g FeS04?7H20样品加热,其受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则下列叙述中不正确的是( )
取8.34g FeS04?7H20样品加热,其受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则下列叙述中不正确的是( )| A、温度为78℃时固体物质M的化学式为FeSO4?4H2O | ||||
| B、温度为l59℃时固体物质N的化学式为FeSO4?H2O | ||||
C、在隔绝空气条件下,N得到P的化学方程式为:FeSO4
| ||||
| D、固体P隔绝空气加热至650℃,得到一种固体物质Q,同时有三种无色气体生成,Q的化学式为Fe2O3 |
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图:
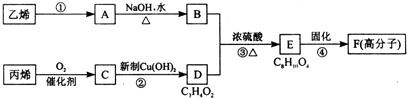
关于该过程的相关叙述正确的是( )

关于该过程的相关叙述正确的是( )
| A、反应④的反应类型是缩聚反应 |
| B、物质A是卤代烃 |
| C、物质B催化氧化后可以得到乙醛 |
| D、1 mol物质D最多可以消耗2 mol NaOH |
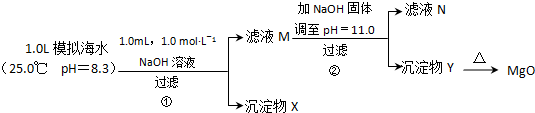
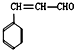 和化合物Ⅱ
和化合物Ⅱ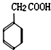 在一定条件下发生反应能生成化合物Ⅲ
在一定条件下发生反应能生成化合物Ⅲ ,请回答以下问题.
,请回答以下问题.