题目内容
如图两瓶体积相等的气体在同温同压时瓶内气体关系一定正确的是( )
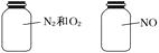
A.相同的质量 B.相同的摩尔质量
C.相同的密度 D.相同的原子数
练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
1.硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等.其部分性质如下表:
回答下列问题:
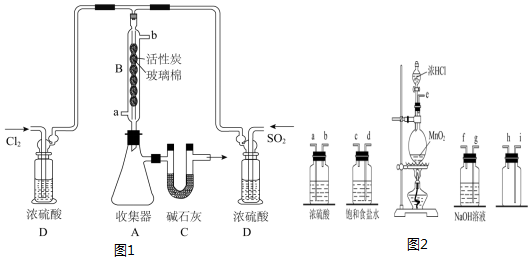
I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如图1:
(1)上述仪器的连接顺序是:e接d,c接a,b接i,h接j(按气流方向,用小写字母表示).
II.催化合成硫酰氯的实验装置如图 2(夹持仪器已省略):
(2)仪器B冷却水的进口为a(填“a””或“b”),活性炭的作用是催化剂.
(3)装置D除干燥气体外,另一作用是通过观察气泡控制气体流速.若缺少D,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?合理,防止硫酰氯分解
(5)C处U形管中碱石灰的作用是吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解.
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯.化学方程式为:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,此法得到的产品中混有硫酸.
(6)①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
| 物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2$\frac{\underline{\;△\;}}{\;}$SO2↑+Cl2↑ |

I.实验室合成硫酰氯需要先制取干燥氯气,制备干燥纯净的氯气所用仪器如图1:
(1)上述仪器的连接顺序是:e接d,c接a,b接i,h接j(按气流方向,用小写字母表示).
II.催化合成硫酰氯的实验装置如图 2(夹持仪器已省略):
(2)仪器B冷却水的进口为a(填“a””或“b”),活性炭的作用是催化剂.
(3)装置D除干燥气体外,另一作用是通过观察气泡控制气体流速.若缺少D,则硫酰氯会水解,该反应的化学方程式为SO2Cl2+2H2O═H2SO4+2HCl.
(4)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么?合理,防止硫酰氯分解
(5)C处U形管中碱石灰的作用是吸收多余二氧化硫、氯气,防止污染;防止水蒸气进入收集器使产品水解.
III.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯.化学方程式为:2ClSO3H$\frac{\underline{催化剂}}{△}$H2SO4+SO2Cl2,此法得到的产品中混有硫酸.
(6)①从分解产物中分离出硫酰氯的方法是蒸馏.
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
取适量产品充分加热后加水稀释,分成两份,一份滴加紫色石蕊试液变红,另一份加入BaCl2溶液产生白色沉淀,说明含有H2SO4.
2.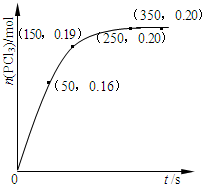 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
 温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )
温度为T时,向2.0L恒容密闭容器中充入1.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据如图.下列说法正确的是( )| A. | 反应在前50 s 的平均速率v(PCl3)=0.0032 mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0mol Cl2,达到平衡时,PCl3 的转化率小于80% | |
| D. | 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3 和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) |
5.某同学需要用450mL 0.2000mol/L NaOH 溶液进行中和滴定实验,请你帮助他完成该溶液配制的相关实验步骤.
(1)他需要选择的主要仪器有托盘天平(砝码)、500mL容量瓶、胶头滴管、药匙、烧杯和玻璃棒;玻璃棒的作用是搅拌和引流.
(2)进行实验:
①该同学通过计算需要准确称量4.0g NaOH固体;
②将称量好的NaOH固体放在小烧杯中,加适量水使其溶解并恢复至室温;
③将溶液转移至事先试过漏的仪器中;
④用适量的蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转入容器中;
⑤定容:先沿着玻璃棒向容量瓶中加入蒸馏水至距离刻度线1~2cm处,再改用胶头滴管滴加蒸馏水至凹液面与刻度线水平相切(填操作过程);
⑥振荡、摇匀、转移、装瓶.
(3)由于该同学态度不够端正,所以在实验过程中出现了一些不规范的操作,请你帮他认真分析一下这些操作对所配制溶液的浓度会造成怎样的影响,并将结果填入下表空白(填“偏高”、“偏低”或“无影响”).
(1)他需要选择的主要仪器有托盘天平(砝码)、500mL容量瓶、胶头滴管、药匙、烧杯和玻璃棒;玻璃棒的作用是搅拌和引流.
(2)进行实验:
①该同学通过计算需要准确称量4.0g NaOH固体;
②将称量好的NaOH固体放在小烧杯中,加适量水使其溶解并恢复至室温;
③将溶液转移至事先试过漏的仪器中;
④用适量的蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转入容器中;
⑤定容:先沿着玻璃棒向容量瓶中加入蒸馏水至距离刻度线1~2cm处,再改用胶头滴管滴加蒸馏水至凹液面与刻度线水平相切(填操作过程);
⑥振荡、摇匀、转移、装瓶.
(3)由于该同学态度不够端正,所以在实验过程中出现了一些不规范的操作,请你帮他认真分析一下这些操作对所配制溶液的浓度会造成怎样的影响,并将结果填入下表空白(填“偏高”、“偏低”或“无影响”).
| 操 作 | 溶液浓度 |
| 砝码放在左盘、NaOH固体放右盘进行称量(1g以下使用游码) | ① |
| 转移溶液时有少量液体洒落到容器外 | ② |
| 定容时俯视刻度线 | ③ |
| 摇匀后观察到液面低于刻度线,立即补充水到凹液面与刻度线水平相切 | ④ |
6.某同学在实验报告中记录下列数据,其中不正确的是( )
| A. | 用托盘天平称取3.2gNaCl固体 | B. | 用10mL量筒量取7.5mL稀盐酸 | ||
| C. | 用450mL的容量瓶配制450mL溶液 | D. | 用广泛pH试纸测得某溶液的pH为3 |


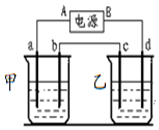 按如图的实验装置进行实验,其中a、b、c、d均为惰性电极.电解质溶液分别为硫酸铜和饱和氯化钠溶液,通电一段时间后,根据下列现象作出判断:【假设电解质均足量】
按如图的实验装置进行实验,其中a、b、c、d均为惰性电极.电解质溶液分别为硫酸铜和饱和氯化钠溶液,通电一段时间后,根据下列现象作出判断:【假设电解质均足量】 1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖.氨的合成不仅解决了地球上因粮食不足而导致的饥饿与死亡问题,在国防、能源、轻工业方面也有广泛用途.
1905年德国化学家哈伯发明了合成氨的方法,他因此获得了1918年度诺贝尔化学奖.氨的合成不仅解决了地球上因粮食不足而导致的饥饿与死亡问题,在国防、能源、轻工业方面也有广泛用途.