题目内容
20.(1)元素M 的离子与NH4+所含电子数和质子数均相同,则M的原子结构示意图为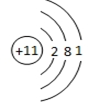 .
.(2)硫酸铝溶液与过量氨水反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(3)能证明Na2SO3溶液中存在SO32-+H2O?HSO3-+OH-水解平衡的事实是C (填序号).
A.滴人酚酞溶液变红,再加人H2SO4溶液后红色退去
B.滴人酚酞溶液变红,再加人氯水后红色退去
C.滴人酚酞溶液变红,再加人BaCl2溶液后产生沉淀且红色退去
(4)元素X、Y 在周期表中位于同一主族,化合物Cu2X和Cu2Y 可发生如下转化(其中D 是纤维素水解的最终产物):Cu2X$\stackrel{过量浓硝酸}{→}$澄清溶液$\stackrel{一定量NaOH溶液}{→}$悬浊液$→_{△}^{D的溶液}$Cu2Y(砖红色沉淀)
①非金属性X<Y(填“>”或“<”)
②Cu2Y与过量浓硝酸反应有红棕色气体生成,化学方程式为Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O
(5)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.
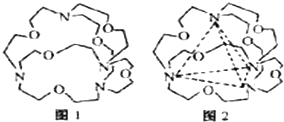
下列分子或离子中,能被该有机化合物识别的是c(填标号).
a.CF4 b.CH4 c.NH4+ d.H2O.
分析 (1)N的质子数为7,H的质子数为1,所以NH4+中质子数为11,电子数为10个,据此解答;
(2)硫酸铝溶液与氨水反应可生成氢氧化铝沉淀和硫酸铵;
(3)如果亚硫酸钠不水解,则溶液中氢氧根离子和氢离子浓度相等,溶液呈中性,向溶液中加入酚酞后溶液不变色,加入和亚硫酸根离子反应的物质后,溶液红色褪色,则证明存在水解平衡;
(4)①采用逆推法,悬浊液与D的溶液(葡萄糖溶液)生成砖红色沉淀是氧化亚铜,推出X、Y元素,再解答;
②Cu2Y为氧化亚铜,+1价的铜具有还原性,硝酸具有氧化性,根据得失电子守恒配平;
(5)能被该有机物识别即能嵌入空腔形成4个氢键,则要求某分子或离子是正四面体结构且能形成氢键,据此解题.
解答 解:(1)N的质子数为7,H的质子数为1,NH4+中含有10个电子,11个质子,与之相同的单核离子为钠离子,则M的原子结构示意图为 ,
,
故答案为: ;
;
(2)硫酸铝溶液与氨水反应可生成氢氧化铝沉淀和硫酸铵,氢氧化铝不能溶于弱碱,则该反应为Al2(SO4)3+6NH3.H2O═2Al(OH)3↓+3(NH4)2SO4,其离子反应为2Al3++3NH3.H2O═2Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(3)A.滴入酚酞试液变红,说明溶液呈碱性,再加入硫酸溶液后,生成具有漂白性的SO2,溶液褪色,不能说明存在SO32-+H2O?HSO3-+OH-水解平衡,故A错误;
B.滴入酚酞试液变红,再加入氯水后,氯气和水反应生成盐酸和次氯酸,次氯酸具有漂白性,能使红色褪色,氯气具有强氧化性,Cl2+SO32-+H2O═SO42-+2Cl-+2H+,Cl2+HSO3-+H2O═SO4 2-+2Cl-+3H+,氯气和碱发生歧化反应,Cl2+2OH-═ClO-+Cl-+H2O,溶液褪色,不能说明存在SO32-+H2O?HSO3-+OH-水解平衡,故B错误;
C.滴入酚酞试液变红,说明溶液中氢氧根离子浓度大于氢离子浓度,再加入氯化钡溶液后,钡离子和亚硫酸根离子反应而和亚硫酸氢根离子不反应,钡离子和亚硫酸根离子反应生成亚硫酸钡沉淀,且溶液红色褪去,所以说明存在SO32-+H2O?HSO3-+OH-水解平衡,故C正确;
故选C;
(4)①根据悬浊液与D的溶液(葡萄糖溶液)生成砖红色沉淀是氧化亚铜,推出Y为O元素,再根据X,Y同主族,推出X为S元素,同一主族,从上往下,非金属性在逐渐减弱,所以,非金属性X<Y;
故答案为:<;
②Cu2Y为氧化亚铜,Cu2O与浓硝酸反应生成红棕色的气体NO2,利用氧化还原反应原理配平,该反应的方程式为:Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O,
故答案为:Cu2O+6HNO3(浓)=2Cu(NO3)2+2NO2↑+3H2O;
(5)要形成氢键,就要掌握形成氢键的条件:一是要有H原子,二是要电负性比较强,半径比较小的原子比如F、O、N等构成的分子间形成的特殊的分子间作用力.符合这样的选项就是C和D,但题中要求形成4个氢键,氢键具有饱和性,这样只有选C.
故选c.
点评 本题较为综合,主要考查推断和逻辑分析能力,明确物质的性质及发生的化学反应是解答的关键,题目难度中等.

| A. | 三氯化铁溶液中加入铁粉 Fe3++Fe═2 Fe2+ | |
| B. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| C. | FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| 物质 | 试剂 | 分离方法 | |
| ① | 氯化钠(硝酸钾) | 蒸馏水 | 降温结晶 |
| ② | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| ③ | 乙醇(水) | 生石灰 | 蒸馏 |
| ④ | 苯(苯酚) | 浓溴水 | 分液 |
| A. | ②③ | B. | ①③ | C. | 只有③ | D. | ③④ |
| ① | ② | ③ | 实验结论 | 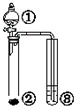 | |
| A. | 硫酸 | Na2SO3 | KMnO4 | SO2有漂白性 | |
| B. | Br2的苯溶液 | 铁屑 | AgNO3 | 苯和溴单质在铁催化剂作用下发生取代反应 | |
| C. | H2O | 工业电石 | KMnO4 | 乙炔具有还原性 | |
| D. | 硫酸 | Na2CO3 | Na2SiO3 | 非金属性:S>C>Si |
| A. | A | B. | B | C. | C | D. | D |
| A. | 观察 | B. | 实验 | C. | 假说 | D. | 模型 |

| A. | 洗涤粗汞可用5%的盐酸代替5%的硝酸 | |
| B. | 辰砂与氧化钙加热反应时,CaSO4为氧化产物 | |
| C. | “灼烧辰砂法”过程中电子转移的方向和数目可表示为: | |
| D. | 减压蒸馏的目的是降低汞的沸点,提高分离效率 |
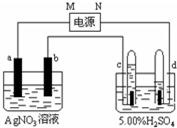 如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.试管充满水,通电一段时间后,在c、d两极上共收集到标准状态下336mL气体,体积如图所示.请回答下列问题.
如图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.试管充满水,通电一段时间后,在c、d两极上共收集到标准状态下336mL气体,体积如图所示.请回答下列问题.