��Ŀ����
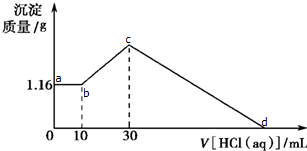 ��m g��NaOH��MgCl2��AlCl3���ֹ�����ɵĻ����Ͷ������ˮ�У��õ�һ����Һ����������Һ��Ϊ���ȷݣ�һ�ݾ����ˡ�ϴ�ӡ������1.16g��ɫ����������һ������Һ����μ���1mol?L-1��HCl��Һ������HCl��Һ����������ɳ�����������ϵ��ͼ��ʾ��
��m g��NaOH��MgCl2��AlCl3���ֹ�����ɵĻ����Ͷ������ˮ�У��õ�һ����Һ����������Һ��Ϊ���ȷݣ�һ�ݾ����ˡ�ϴ�ӡ������1.16g��ɫ����������һ������Һ����μ���1mol?L-1��HCl��Һ������HCl��Һ����������ɳ�����������ϵ��ͼ��ʾ����1������Һ�г�ˮ�⣬�����е�������
��2��ab�η�����Ӧ�Ļ�ѧ����ʽ��
��3��ԭ�������MgCl2��������
��4��d������������
���㣺�йػ���ﷴӦ�ļ���
ר�⣺������
�������������ɵĻ������Һ�м�������ʱ��a-bʱû�г������ɣ�˵����Һ��NaOH����������������ȫת��Ϊƫ��������ӣ���Һ�д��ڵij���ΪMg��OH��2��
b-c�Σ������ƫ�����Ʒ�Ӧ���������������������ӷ�Ӧ����ʽΪH2O+AlO2-+H+=Al��OH��3����c����Һ�д��ڵ��������Ȼ��ƣ�����ΪMg��OH��2��Al��OH��3��
c-d�����У�������þ�����������������ᷴӦ�����Ȼ������Ȼ�þ������d����Һ�е��������Ȼ������Ȼ�þ���Ȼ��ƣ��ݴ˽���������ݽ��н��
b-c�Σ������ƫ�����Ʒ�Ӧ���������������������ӷ�Ӧ����ʽΪH2O+AlO2-+H+=Al��OH��3����c����Һ�д��ڵ��������Ȼ��ƣ�����ΪMg��OH��2��Al��OH��3��
c-d�����У�������þ�����������������ᷴӦ�����Ȼ������Ȼ�þ������d����Һ�е��������Ȼ������Ȼ�þ���Ȼ��ƣ��ݴ˽���������ݽ��н��
���
�⣺��1���������ɵĻ������Һ�м�������ʱ��a-bʱû�г������ɣ�˵����Һ��NaOH��������Һ����������ȫת��Ϊƫ��������ӣ�
��Һ�д��ڵij���ΪMg��OH��2����������Һ�г���ˮ���������NaAlO2��Mg��OH��2��������NaOH��
�ʴ�Ϊ��NaAlO2��Mg��OH��2��NaOH��
��2��a-b�μ����������������������Ʒ�Ӧ����Ӧ�� ��ѧ����ʽΪ��NaOH+HCl=NaCl+H2O��
b-c�������ƫ�����Ʒ�Ӧ���������������������ӷ�Ӧ����ʽΪ��H2O+AlO2-+H+=Al��OH��3����
�ʴ�Ϊ��NaOH+HCl=NaCl+H2O��H2O+AlO2-+H+=Al��OH��3����
��3��a���������������þ����n[Mg��OH��2]=
=0.02mol������Mgԭ���غ�ã�n��MgCl2��=n[Mg��OH��2]=0.02mol���Ȼ�þ������Ϊ��0.02mol��95g/mol=1.9g��
b-c�Σ������ƫ�����Ʒ�Ӧ���������������������ӷ�Ӧ����ʽΪ��H2O+AlO2-+H+=Al��OH��3��������HCl�����֪��n��AlO2-��=n��HCl��=1mol/L����0.03-0.01��L=0.02mol��������ԭ���غ�ã�n��AlCl3��=n��AlO2-��=0.02mol���Ȼ���������Ϊ��0.02mol��133.5g/mol=2.67g��
c��ʱ����Ϊ�Ȼ��ƣ���Na+���Ӻ�Cl-�����غ�ã�ԭ�������n��NaOH��=n��NaCl��=n��Cl-��=2n��MgCl2��+3n��AlCl3��+n��HCl��=0.02mol��2+0.02mol��3+0.03L��1mol/L=0.13mol���������Ƶ�����Ϊ��0.13mol��40g/mol=5.2g��
���Ի�������Ȼ�������������Ϊ��
��100%��27.3%��
�ʴ�Ϊ��1.9��27.3%��
��3��c-d�����У�������þ�����������������ᷴӦ�����Ȼ������Ȼ�þ������d����Һ�е��������Ȼ������Ȼ�þ���Ȼ��ƣ�ʵ�����൱���������ƺ�����ķ�Ӧ�����Զ���ǡ�÷�Ӧʱn��NaOH��=n��HCl������������������Ϊ��V=
=0.13L=130mL��
�ʴ�Ϊ��130��
��Һ�д��ڵij���ΪMg��OH��2����������Һ�г���ˮ���������NaAlO2��Mg��OH��2��������NaOH��
�ʴ�Ϊ��NaAlO2��Mg��OH��2��NaOH��
��2��a-b�μ����������������������Ʒ�Ӧ����Ӧ�� ��ѧ����ʽΪ��NaOH+HCl=NaCl+H2O��
b-c�������ƫ�����Ʒ�Ӧ���������������������ӷ�Ӧ����ʽΪ��H2O+AlO2-+H+=Al��OH��3����
�ʴ�Ϊ��NaOH+HCl=NaCl+H2O��H2O+AlO2-+H+=Al��OH��3����
��3��a���������������þ����n[Mg��OH��2]=
| 1.16g |
| 58g/mol |
b-c�Σ������ƫ�����Ʒ�Ӧ���������������������ӷ�Ӧ����ʽΪ��H2O+AlO2-+H+=Al��OH��3��������HCl�����֪��n��AlO2-��=n��HCl��=1mol/L����0.03-0.01��L=0.02mol��������ԭ���غ�ã�n��AlCl3��=n��AlO2-��=0.02mol���Ȼ���������Ϊ��0.02mol��133.5g/mol=2.67g��
c��ʱ����Ϊ�Ȼ��ƣ���Na+���Ӻ�Cl-�����غ�ã�ԭ�������n��NaOH��=n��NaCl��=n��Cl-��=2n��MgCl2��+3n��AlCl3��+n��HCl��=0.02mol��2+0.02mol��3+0.03L��1mol/L=0.13mol���������Ƶ�����Ϊ��0.13mol��40g/mol=5.2g��
���Ի�������Ȼ�������������Ϊ��
| 2.67g |
| 1.9g+2.67g+5.2g |
�ʴ�Ϊ��1.9��27.3%��
��3��c-d�����У�������þ�����������������ᷴӦ�����Ȼ������Ȼ�þ������d����Һ�е��������Ȼ������Ȼ�þ���Ȼ��ƣ�ʵ�����൱���������ƺ�����ķ�Ӧ�����Զ���ǡ�÷�Ӧʱn��NaOH��=n��HCl������������������Ϊ��V=
| 0.13mol |
| 1mol/L |
�ʴ�Ϊ��130��
���������⿼�����ﷴӦ�ļ��㣬��Ŀ�Ѷ��еȣ���ȷ���߱仯���Ƽ�ÿ�η����Ļ�ѧ��Ӧ�ǽⱾ��ؼ���֪��������Һ�ж�Ӧ��������ʲô���ٽ��ԭ���غ�����������״����ǣ�3�������Դ������ϻ�ѧʽ�仯���������Ӷ��ó���ȷ�𰸣�

��ϰ��ϵ�д�
 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
�����Ŀ
�Ѷ����к��������Ȼ���-COOH��������ʽΪC6H10O4�����Ѷ�����ܵĽṹ�У������������칹����������
| A��7�� | B��8�� | C��9�� | D��10�� |
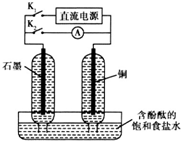 ij��ȤС�������ͼ��ʵ��װ�ã�ʵ��ʱ���ȶϿ�K2���պ�K1�������������ݲ�����һ��ʱ��Ͽ�K1���պ�K2�����ֵ�����Aָ��ƫת�������й�������ȷ���ǣ�������
ij��ȤС�������ͼ��ʵ��װ�ã�ʵ��ʱ���ȶϿ�K2���պ�K1�������������ݲ�����һ��ʱ��Ͽ�K1���պ�K2�����ֵ�����Aָ��ƫת�������й�������ȷ���ǣ�������| A���Ͽ�K2���պ�K1ʱ��ͭ�缫Ϊ���� |
| B���Ͽ�K2���պ�K1ʱ��ʯī�缫������Һ��� |
| C���Ͽ�K1���պ�K2ʱ��ͭ�缫������ԭ��Ӧ |
| D���Ͽ�K1���պ�K2ʱ��ʯī�缫������ |
 ��
��