题目内容
短周期原子序数依次递增的A、B、C、D、E、F六种元素,已知B原子最外层电子数是A原子次外层电子数的3倍,是D原子最外层电子数的2倍;C原子内层电子总数是最外层电子数10倍;A、B、D三种元素的原子最外层电子数之和为13;A和B原子最外层电子数之和与D和F原子最外层电子数之和相等;D和E是相邻两种元素.
(1)E元素基态原子的核外电子占用了 个原子轨道.
(2)A、B、C三种元素组成原子个数比为n(A):n(B):n(C)=1:3:2的化合物,该化合物的水溶液显 (填“酸性”“碱性”“中性”),原因用离子方程式可表示为 .
(3)B、C、D三种元素离子半径最小的是 (填离子符号);AB2分子的电子式是 .M元素与D元素位于不同主族,但由于二者的电负性相近,导致某些性相似,将M的最高价氧化物溶于C的氢氧化物的水溶液中,发生反应的离子方程式为 .
(4)E和F形成的化合物X容易水解生成两种酸,写出该水解反应的化学方程式 .
(1)E元素基态原子的核外电子占用了
(2)A、B、C三种元素组成原子个数比为n(A):n(B):n(C)=1:3:2的化合物,该化合物的水溶液显
(3)B、C、D三种元素离子半径最小的是
(4)E和F形成的化合物X容易水解生成两种酸,写出该水解反应的化学方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:已知B原子最外层电子数是A原子次外层电子数的3倍,是D原子最外层电子数的2倍,说明B元素最外层电子数为6,D原子最外层电子数为3,A的次外层电子数为2;C原子内层电子总数是最外层电子数10倍,则C为Na;A、B、D三种元素的原子最外层电子数之和为13,则A的最外层为13-6-3=4,所以A的核外电子数为2+4=6为C元素;A和B原子最外层电子数与D和F原子最外层电子数之和相等,则F的最外层为7,F的原子序数最大,应为Cl元素;D和E是相邻两种元素,D原子最外层电子数为3,所以D为Al元素,E为Si元素;B元素最外层电子数为6,且原子序数比Na小,则为O元素,综上可知:A为C元素,B为O元素,C为Na元素,D为Al元素,E为Si元素,F为Cl元素;结合元素对应单质化合物的性质以及元素周期律解答该题.
解答:
解:已知B原子最外层电子数是A原子次外层电子数的3倍,是D原子最外层电子数的2倍,说明B元素最外层电子数为6,D原子最外层电子数为3,A的次外层电子数为2;C原子内层电子总数是最外层电子数10倍,则C为Na;A、B、D三种元素的原子最外层电子数之和为13,则A的最外层为13-6-3=4,所以A的核外电子数为2+4=6为C元素;A和B原子最外层电子数与D和F原子最外层电子数之和相等,则F的最外层为7,F的原子序数最大,应为Cl元素;D和E是相邻两种元素,D原子最外层电子数为3,所以D为Al元素,E为Si元素;B元素最外层电子数为6,且原子序数比Na小,则为O元素,综上可知:A为C元素,B为O元素,C为Na元素,D为Al元素,E为Si元素,F为Cl元素;
(1)已知E为Si元素,Si元素的原子核外有14个电子,其电子排布式为:1s22s22p63s23p2,2个电子占据一个原子轨道,其中3p轨道上的2个电子,各占一个轨道,所以共占据8个原子轨道;
故答案为:8;
(2)由A、B、C三种元素组成原子个数比nA:nB:nC=1:3:2的化合物为Na2CO3,碳酸钠中的碳酸根离子会发生水解反应,即CO32-+H2O?HCO3-+OH-,所以Na2CO3溶液呈碱性,
故答案为:碱性;CO32-+H2O?HCO3-+OH-;
(3)B为O元素,C为Na元素,D为Al元素,它们的离子核外电子数相同,原子序数越大,离子半径越小,则Al3+的半径最小;AB2分子为CO2,是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ;BeO与氢氧化钠反应生成BeO22-和H2O,其离子方程式为:BeO+2OH-=BeO22-+H2O;
;BeO与氢氧化钠反应生成BeO22-和H2O,其离子方程式为:BeO+2OH-=BeO22-+H2O;
故答案为:Al3+; ;BeO+2OH-=BeO22-+H2O;
;BeO+2OH-=BeO22-+H2O;
(5)E和F形成的化合物X为SiCl4,SiCl4与水反应生成HCl和硅酸,其反应的方程式为为:气制取高纯度的单质Si的化学原理是:SiCl4+3H2O=H2SiO3↓+4HCl,
故答案为:SiCl4+3H2O=H2SiO3↓+4HCl.
(1)已知E为Si元素,Si元素的原子核外有14个电子,其电子排布式为:1s22s22p63s23p2,2个电子占据一个原子轨道,其中3p轨道上的2个电子,各占一个轨道,所以共占据8个原子轨道;
故答案为:8;
(2)由A、B、C三种元素组成原子个数比nA:nB:nC=1:3:2的化合物为Na2CO3,碳酸钠中的碳酸根离子会发生水解反应,即CO32-+H2O?HCO3-+OH-,所以Na2CO3溶液呈碱性,
故答案为:碱性;CO32-+H2O?HCO3-+OH-;
(3)B为O元素,C为Na元素,D为Al元素,它们的离子核外电子数相同,原子序数越大,离子半径越小,则Al3+的半径最小;AB2分子为CO2,是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为
 ;BeO与氢氧化钠反应生成BeO22-和H2O,其离子方程式为:BeO+2OH-=BeO22-+H2O;
;BeO与氢氧化钠反应生成BeO22-和H2O,其离子方程式为:BeO+2OH-=BeO22-+H2O;故答案为:Al3+;
 ;BeO+2OH-=BeO22-+H2O;
;BeO+2OH-=BeO22-+H2O;(5)E和F形成的化合物X为SiCl4,SiCl4与水反应生成HCl和硅酸,其反应的方程式为为:气制取高纯度的单质Si的化学原理是:SiCl4+3H2O=H2SiO3↓+4HCl,
故答案为:SiCl4+3H2O=H2SiO3↓+4HCl.
点评:本题考查的是有关核外电子排布的推断题,此类型题的解题规律是:先根据题干信息推断元素,再根据元素化合物知识解决有关问题,题目难度中等,侧重于电子排布和元素周期律知识的综合应用的考查.

练习册系列答案
相关题目
1.52g铜镁合金完全溶解于足量的稀硝酸中,充分反应后,加入足量的NaOH溶液,经过过滤、洗涤、干燥后称得固体质量为2.54g,问生成的气体在标准状况下的体积 L,镁的物质的量是 ,铜的物质的量是 .
实验室中,有关试剂的保存方法错误的是( )
| A、浓硝酸保存在棕色细口瓶中 |
| B、液溴用水封保存 |
| C、少量金属钠保存在煤油中 |
| D、烧碱溶液保存在带玻璃塞的试剂瓶中 |
下列物质中不易被酸雨腐蚀的是( )
| A、铜像 | B、大理石雕塑 |
| C、水泥路面 | D、铝制窗台 |
 X、Y、M、Z、W为原子序数依次增大的五种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水.
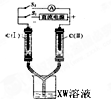
X、Y、M、Z、W为原子序数依次增大的五种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水.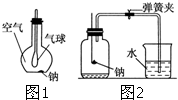 (1)如图1所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气.过一段时间后可观察到
(1)如图1所示装置,在平底烧瓶的底部有一块钠,平底烧瓶内是干燥的空气.过一段时间后可观察到