题目内容
4.下列有关物质性质或应用的说法正确的是( )| A. | 制水泥和玻璃都用石灰石作原料 | |
| B. | 利用Al2O3制作的坩埚,可用于熔融烧碱 | |
| C. | Si可用作太阳能电池和光导纤维的材料 | |
| D. | 铜的金属活泼性比铁的弱,铜不能与任何强酸发生反应 |
分析 A.水泥原料是石灰石和黏土;玻璃原料是纯碱、石灰石和石英;
B.氧化铝为两性氧化物能够与氢氧化钠反应;
C.二氧化硅是制作光导纤维的原料;
D.铜与硝酸能发生氧化还原反应.
解答 解:A.水泥原料是石灰石和黏土;玻璃原料是纯碱、石灰石和石英,制水泥和玻璃都用石灰石作原料,故A正确;
B.氧化铝为两性氧化物能够与氢氧化钠反应生成偏铝酸钠,故B错误;
C.Si可用作太阳能电池,二氧化硅是制作光导纤维的原料,故C错误;
D.铜与稀硝酸反应生成硝酸铜、水和一氧化氮,故D错误;
故选A.
点评 本题考查了元素及化合物知识,题目难度不大,熟悉氧化铝的性质是解题关键,注意制备水泥玻璃的原料.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
14.下列装置或操作能达到实验目的是( )
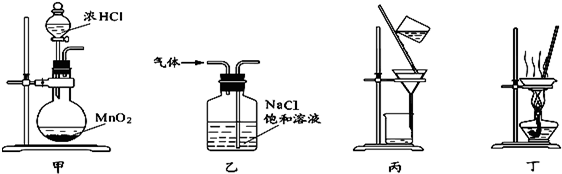

| A. | 用装置甲制取氯气 | |
| B. | 用装置乙除去氯气中的少量氯化氢 | |
| C. | 用装置丙分离二氧化锰和氯化锰溶液 | |
| D. | 用装置丁将饱和食盐水完全蒸干制NaCl |
15.取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是( )
①金属先熔化
②在空气中燃烧,放出黄色火花
③燃烧后得白色固体
④燃烧时火焰为黄色
⑤燃烧后生成浅黄色固体物质.
①金属先熔化
②在空气中燃烧,放出黄色火花
③燃烧后得白色固体
④燃烧时火焰为黄色
⑤燃烧后生成浅黄色固体物质.
| A. | ②⑤ | B. | ①②③ | C. | ①④⑤ | D. | ④⑤ |
12.元素的最高价氧化物溶于水,形成的含氧酸的酸性最强的是( )
| A. | 原子最外层电子数是次外层的2倍的元素 | |
| B. | 原子M层电子数等于另两层电子数之差的元素 | |
| C. | 第三周期ⅦA族的元素 | |
| D. | 其单质有多种同素异形体,其中一种着火点很低、能自燃的元素 |
13.25℃时,已知0.5mol/L的HA溶液pH=3,现向10mL的HA溶液中滴加一定体积的amol•L-1的NaOH溶液,下列有关说法中错误的是( )
| A. | 25℃时HA溶液的电力平衡常数约为2×10-6 | |
| B. | 当滴入10mLNaOH时溶液恰好为中性,则a<0.5mol•L-1 | |
| C. | 滴加过程中,溶液中的离子浓度有可能为c(Na+)=c(A-) | |
| D. | 滴加过程中,溶液中的离子浓度关系不可能有c(A-)>c(H+)>c(Na+)>c(OH-) |
7.向27.2g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2.在所得溶液中加入1.0molL-1的NaOH溶液1.0L,此时溶液呈中性,金属铜离子已完全沉淀,沉淀质量为39.2g.下列有关说法不正确的是( )
| A. | Cu与Cu2O的物质的量之比为2:1 | |
| B. | 沉淀为氢氧化铜 | |
| C. | 产生的NO在标准状况下的体积为4.48 L | |
| D. | Cu、Cu2O与硝酸恰好完全反应 |