题目内容
下列各组物质中,互为同素异形体的是( )
| A、氕和氘 | B、水和重水 |
| C、纯碱和烧碱 | D、石墨和金刚石 |
考点:同素异形体
专题:
分析:根据同素异形体是同种元素形成的不同单质,同素异形体首先是单质,其次是同种元素,利用该知识分析判断即可.
解答:
解:A.氕和氘分别为11H和12H,它们的质子数都为1,中子数不同分别为0、1,是氢元素的不同原子,互为同位素,故A错误;
B.H2O和D2O都是化合物,不属于同素异形体,故B错误;
C.纯碱和烧碱都是化合物,不属于同素异形体,故C错误;
D.石墨和金刚石都是由碳元素组成的不同单质,属于同素异形体,故D正确;
故选D.
B.H2O和D2O都是化合物,不属于同素异形体,故B错误;
C.纯碱和烧碱都是化合物,不属于同素异形体,故C错误;
D.石墨和金刚石都是由碳元素组成的不同单质,属于同素异形体,故D正确;
故选D.
点评:本题考查同素异形体的判断,难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,②不同单质,这是解决此类题的关键之所在.

练习册系列答案
相关题目
如图为阳离子交换膜法电解饱和食盐水原理示意图.下列说法不正确的是( )
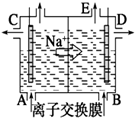

| A、完全电解后加适量盐酸可以恢复到电解前的浓度 |
| B、从B中加入含少量NaOH的水溶液以增强导电性 |
| C、标准状况下每生成22.4 L Cl2,使产生2 mol NaOH |
| D、从E口逸出的气体是H2 |
NA代表阿伏加德罗常数,下列说法不正确的是( )
| A、标准状况下,11.2L氯仿(CHCl3)中含有C-Cl键的数目为1.5NA |
| B、常温常压下,15g甲基(-CH3)所含的电子数为9NA |
| C、同温同压下,1LNO和1LO2充分混合体积小于1.5L |
| D、pH=l的醋酸溶液100mL中氢离子数为0.01 NA |
设NA为何伏加德罗常数的值,下列叙述正确的是( )
| A、1mol甲醇中含有C-H键数目为4NA |
| B、室温下,PH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C、标准状况下,2.24L已烷含有的分子数目为0.1NA |
| D、常温常压下,46gNO2和N2O4的混合气体中含有的原子数为3NA |
在化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的情况,下列反应中属于这种情况的是( )
①过量的锌与浓硫酸反应;
②过量的氢气与少量的N2在工业生产条件下反应;
③过量的浓盐酸与碳酸钙反应;
④过量的乙酸和少量乙醇在浓硫酸、加热条件下反应;
⑤过量二氧化锰与浓盐酸在加热条件下反应;
⑥过量的铜与浓硫酸在加热条件下反应.
①过量的锌与浓硫酸反应;
②过量的氢气与少量的N2在工业生产条件下反应;
③过量的浓盐酸与碳酸钙反应;
④过量的乙酸和少量乙醇在浓硫酸、加热条件下反应;
⑤过量二氧化锰与浓盐酸在加热条件下反应;
⑥过量的铜与浓硫酸在加热条件下反应.
| A、②③④⑥ | B、①②④⑤ |
| C、②④⑤⑥ | D、③④⑤⑥ |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、0.1mol Fe 与0.1mol Cl2充分反应,转移的电子数为0.3 NA |
| B、常温常压下,1mol的氦气和氢气混合气,含有的核外电子数为2NA |
| C、25℃时,1L pH=13的Ba(OH)2溶液中含有OH-的数目为0.2 NA |
| D、标准状况下,2.24L CCl4和CH2O的混合物中含有NA个碳原子 |
下列化学用语表达正确的是( )
| A、溴化钙的化学式是CaBr |
B、HCl分子的电子式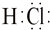 |
| C、乙烯的结构简式:CH2CH2 |
D、氯原子的结构示意图: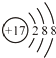 |
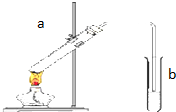 用如图所示的装置制取乙酸乙酯.回答下列问题:
用如图所示的装置制取乙酸乙酯.回答下列问题: