题目内容
15.某温度下,2L密闭容器中加入4mol A和2mol B发生反应:3A(g)+2B(g)═4C(s)+2D(g).平衡时测得n(C)=1.6mol.下列说法正确的是( )| A. | 化学平衡常数K=$\frac{{c}^{4}(C)•{c}^{2}(D)}{{c}^{3}(A)•{c}^{2}(B)}$ | |
| B. | 增大压强,平衡右移,K平衡增大 | |
| C. | B的平衡转化率是40% | |
| D. | 其他条件不变,向平衡体系中加入少量C,v正、v逆均增大 |
分析 A.C为固体,不能列入平衡常数表达式中;
B.平衡常数只与温度有关;
C.根据方程式计算转化率;
D.C为固体,增加C的量对反应速率无影响.
解答 解:A.C为固体,不能列入平衡常数表达式中,K=$\frac{{c}^{2}(D)}{{C}^{3}(A){C}^{2}(B)}$,故A错误;
B.平衡常数只与温度有关,温度不变,平衡常数不变,故B错误;
C.由反应的方程式可知,生成n(C)=1.6mol,则消耗B为0.8mol,B的平衡转化率是$\frac{0.8mol}{2mol}$=40%,故C正确;
D.C为固体,增加C的量对反应速率无影响,故D错误.
故选C.
点评 本题考查化学平衡常数,题目难度不大,注意C为固体的特征,为解答该题的关键,也是易错点.

练习册系列答案
相关题目
5.可以用分液漏斗分离的一组液体混合物是( )
| A. | 溴和四氯化碳 | B. | 苯和溴苯 | C. | 汽油和苯 | D. | 溴苯和水 |
6.下列物质中,与苯酚互为同系物的是( )
| A. | 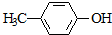 | B. |  | C. |  | D. | C7H8O |
3.下列说法中正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 只含有离子键的化合物才是离子化合物 | |
| C. | 并非只有非金属原子间才能形成共价键 | |
| D. | 由共价键形成的分子一定是共价化合物 |
4.能用H++OH-=H2O来表示的化学反应是( )
| A. | NaOH溶液与碳酸反应 | B. | Cu(OH)2与稀硝酸反应 | ||
| C. | Ba(OH)2溶液与稀硫酸反应 | D. | KOH溶液与稀盐酸反应 |
5.下列各组物质中,化学键类型完全相同的是( )
| A. | HI和NaI | B. | H2O2和CO2 | C. | Cl2和CCl4 | D. | MgCl2和NaBr |
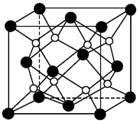 (1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:
(1)原子序数小于36的X、Y、Z、W四种元素,其中X是元素周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题: