题目内容
在一个2L的密闭容器中,放入2mol气体A进行反应,5分钟后,测得这种气体A还剩余0.5mol,则该反应前5分钟气体A的化学反应速率是( )
| A、0.3mol/(L?min) |
| B、0.15mol/(L?min) |
| C、0.75mol/(L?min) |
| D、0.075mol/(L?min) |
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:根据定义式:气体A的化学反应速率v(A)=
=
来计算化学反应的速率即可.
| △c |
| △t |
| ||
| △t |
解答:
解:气体A的化学反应速率v(A)=
=
=
=0.15mol/(L?min).
故选B.
| △c |
| △t |
| ||
| △t |
| ||
| 5min |
故选B.
点评:本题考查学生利用公式计算物质化学反应速率知识,注意公式的掌握和熟练应用是关键,难度不大.

练习册系列答案
相关题目
丙烯醛的结构简式为: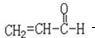 下列试剂中,不能跟丙烯醛反应的( )
下列试剂中,不能跟丙烯醛反应的( )
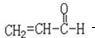 下列试剂中,不能跟丙烯醛反应的( )
下列试剂中,不能跟丙烯醛反应的( )| A、溴水 |
| B、新制的Cu(OH)2 |
| C、Na2CO3溶液 |
| D、KMnO4酸性溶液 |
在恒温恒容的密闭容器中发生反应:Fe3O4(s)+4H2(g)?3Fe(s)+4H2O(g).下列说法正确的是( )
A、该反应的平衡常数表达式K=
| ||
| B、若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态 | ||
| C、若Fe3O4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变 | ||
| D、若初始时投入4.64g Fe3O4与一定量H2,反应达平衡时容器内固体共有4g,则Fe3O4的转化率为50% |
下列有关说法正确的是( )
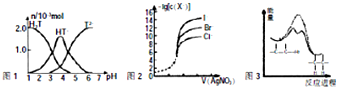

| A、常温下,向20mL 0.1mol?L-1酒石酸(H2T)溶液中添加0.1mol?L-1 NaOH溶液,有关微粒的物质的量与混合溶液的pH关系如图1,则H2T的酸性比H2CO3强 |
| B、用0.0100mol?L-1硝酸根标准溶液,滴定浓度均为0.100mol?L-1的Cl、Br及I的混合溶液,由图2曲线可确定首先沉淀的是Cl- |
| C、碳酸氢钠溶液中存在:c(H+)+2c(H2CO3)=c(OH-)+2c(CO32-) |
| D、由图3可说明烯烃与H2加成反应,虚线表示在催化剂的作用下进行 |
下列物质中,含氢原子数目最多的是( )
| A、0.9molH2O |
| B、0.3molH2SO4 |
| C、0.2molNH3 |
| D、0.4molCH4 |
在托盘天平的两个托盘上分别放有同样大小的两个烧杯,烧杯内部分别装有等量盐酸,天平保持平衡.这时,分别向两个烧杯中加入等质量的下列物质,充分反应后(酸过量),天平仍能保持平衡的是( )
| A、CaCO3和KHCO3 |
| B、Na2CO3和NaHCO3 |
| C、Na2CO3和K2CO3 |
| D、Na2CO3和CaCO3 |
据报道,最近国际上研制出了一种新型锂离子电池,该电池的总反应方程式为Li15Si4+15NiO2
4Si+15LiNiO2.下列说法中正确的是( )
| 放电 |
| 充电 |
| A、放电时,电池内部Li+由正极向负极移动 |
| B、每转移0.4 mol电子,有2.8 g Si发生转化 |
| C、放电时负极得电子,质量减轻 |
| D、充电时,阳极的反应式为LiNiO2-e-═NiO2+Li+ |
下列说法正确的是( )
| A、在常温常压下,11.2LN2含有分子数为0.5NA |
| B、2 g氢气的体积是22.4L |
| C、在标准状况下,1mol的任何气体的体积都约是22.4L. |
| D、在化学反应中,参加反应的各物质的质量比等于其物质的量的比. |