题目内容
7.某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )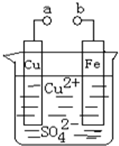
| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铁片上发生的反应为:Fe-3e-=Fe3+ | |
| C. | a和b用导线连接时电子从Cu片流向铁片 | |
| D. | a和b用导线连接时,Cu2+向铜电极移动 |
分析 A.a和b不连接时,铁和铜离子发生置换反应;
B.a和b连接时,该装置构成原电池,铁失电子生成亚铁离子;
C.原电池中电子从负极流出正极;
D.原电池放电时,阳离子向正极移动.
解答 解:A.a和b不连接时,铁和铜离子发生置换反应,所以铁片上有铜析出,故A正确;
B.a和b连接时,该装置构成原电池,铁作负极,铁失电子生成亚铁离子,电极方程式为:Fe-2e-=Fe2+,故B错误;
C.a和b用导线连接时,形成原电池,原电池中电子从负极流出正极,即电子从Fe片流向Cu片,故C错误;
D.a和b连接时,该装置构成原电池,铁作负极,铜作正极,原电池放电时,铜离子向铜电极移动,故D正确;
故选:BC.
点评 本题考查了原电池原理,明确正负极的判断方法、电极反应类型、阴阳离子移动方向即可解答,难度不大,易错点为阴阳离子移动方向的判断.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
17.某化合物有碳、氢、氧三种元素组成,其红外光谱图有C-H键、O-H键、C-O键的振动吸收,该有机物的相对分子质量是60,则该有机物的结构简式( )
| A. | CH3CH2OCH3 | B. | CH3CH(OH)CH3 | C. | CH3CH2 CH2CH2OH | D. | CH3CH2CHO |
18.检验溴乙烷中含有溴元素存在的实验步骤、操作和顺序正确的是( )
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却.
| A. | ①②④③ | B. | ②④③① | C. | ②④① | D. | ③④① |
2.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1 mol D2O所含质子数为12 NA | |
| B. | 1 mol C16H34中的极性键数为34 NA | |
| C. | 10 g 氖气所含原子数为NA | |
| D. | 22.4 L正戊烷含氢原子数为12 NA |
12.化学工业在经济发展中的作用举足轻重,下列有关工业生产的叙述中,正确的是( )
| A. | 硫酸生产中常采用催化剂提高SO2的转化率 | |
| B. | 合成氨中采用及时分离氨气提高反应速率 | |
| C. | 电镀铜时,溶液中c(Cu2+)基本保持不变 | |
| D. | 用电解熔融氧化镁的方法制取镁 |
19.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | 新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | |
| B. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.4mol•L-1CH3COOH溶液与0.2mol•L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
13.①丙烯;②氯乙烯;③苯,三种有机化合物中,分子内所有原子均在同一平面的是( )
| A. | ①② | B. | ②③ | C. | ③ | D. | ② |
 表示的分子式C7H12;名称是3-甲基-2,4-己二烯.
表示的分子式C7H12;名称是3-甲基-2,4-己二烯.