题目内容
下列解释实际应用的原理表达式中,不正确的是
- A.用排饱和食盐水法收集Cl2:Cl2+H2O?H++Cl-+HClO
- B.热的纯碱溶液碱性增强:
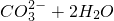 ?
?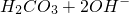
- C.向Mg(OH)2悬浊液中加入FeCl3溶液:
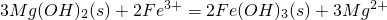
- D.用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量)?TiO2.xH2O↓+4HCl
BC
分析:A.氯气与水的反应为可逆反应;
B.碳酸根离子水解分步进行,以第一步为主;
C.氢氧化铁的溶解度比氢氧化镁的小,沉淀转化为可逆反应;
D.四氯化钛水解生成沉淀和HCl.
解答:A.氯气溶于水发生Cl2+H2O?H++Cl-+HClO,饱和食盐水中氯离子浓度较大,抑制氯气的溶解,故A正确;
B.纯碱溶液存在CO32-+H2O?HCO3-+OH-,水解为吸热反应,加热促进水解,碱性增强,故B错误;
C.氢氧化铁的溶解度比氢氧化镁的小,则向Mg(OH)2悬浊液中加入FeCl3溶液发生3Mg(OH)2(s)+2Fe3+?2Fe(OH)3(s)+3Mg2+,故C错误;
D.四氯化钛水解,则用TiCl4制备TiO2的离子反应为TiCl4+(x+2)H2O(过量)?TiO2.xH2O↓+4HCl,故D正确;
故选BC.
点评:本题考查离子反应方程式的书写,涉及化学平衡、水解平衡、沉淀转化等离子反应,综合性较大,题目难度中等.
分析:A.氯气与水的反应为可逆反应;
B.碳酸根离子水解分步进行,以第一步为主;
C.氢氧化铁的溶解度比氢氧化镁的小,沉淀转化为可逆反应;
D.四氯化钛水解生成沉淀和HCl.
解答:A.氯气溶于水发生Cl2+H2O?H++Cl-+HClO,饱和食盐水中氯离子浓度较大,抑制氯气的溶解,故A正确;
B.纯碱溶液存在CO32-+H2O?HCO3-+OH-,水解为吸热反应,加热促进水解,碱性增强,故B错误;
C.氢氧化铁的溶解度比氢氧化镁的小,则向Mg(OH)2悬浊液中加入FeCl3溶液发生3Mg(OH)2(s)+2Fe3+?2Fe(OH)3(s)+3Mg2+,故C错误;
D.四氯化钛水解,则用TiCl4制备TiO2的离子反应为TiCl4+(x+2)H2O(过量)?TiO2.xH2O↓+4HCl,故D正确;
故选BC.
点评:本题考查离子反应方程式的书写,涉及化学平衡、水解平衡、沉淀转化等离子反应,综合性较大,题目难度中等.

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
4种短周期元素A、B、C、D的相关信息如下:信息①原子半径大小:A>B>C>D信息②4种元素的原子之间形成的甲、乙和丙3种物质的部分信息如下:
| 甲 | 乙 | 丙 | |
| 分子 比例模型 | 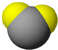 | 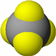 |  |
| 物质性质 | 地球上最常见的物质,是组成生物体的重要物质之一,约占人体质量的2/3. | 无色,无气味并且易燃.是常见的一种基础能源. | 有强氧化性的弱酸,可以用于消毒杀菌. |
(1)元素B在周期表中的位置______,丙分子的电子式______.
(2)元素E、F与元素A处于同一周期,E单质的还原性最强,且与甲能反应生成化合物X.含元素F的某些盐可作为净水剂,由元素F、C组成的化合物Y可作为耐火材料.
①写出元素A的单质与甲反应的化学方程式:______.
②写出化合物Y溶解于X溶液的离子方程式:______.
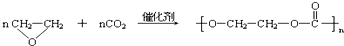
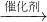 N2+2CO2
N2+2CO2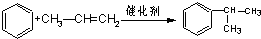
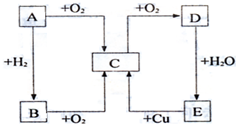 如图所示,A.B.C.D.E为中学化学中常见的五种物质,它们之间有如下相互转化关系
如图所示,A.B.C.D.E为中学化学中常见的五种物质,它们之间有如下相互转化关系