题目内容
某车间有一铁合金,工人师傅不知道是生铁还是钢(已知钢含C量:0.03%-2%,生铁含C量:2%-4.3%),取合金样品1.1g在纯氧中燃烧,得到0.013g二氧化碳,通过计算回答该合金是生铁还是钢?
考点:有关混合物反应的计算
专题:计算题
分析:根据n=
计算出0.13g二氧化碳的物质的量,从而得出合金中C的质量,然后根据m=nM计算出C的质量,再计算出合金中含碳量,最后根据“钢含C量:0.03%-2%,生铁含C量:2%-4.3%”进行判断.
| m |
| M |
解答:
解:0.013g二氧化碳的物质的量为:
≈0.000295mol,
根据质量守恒定律可知合金中C的质量为:12g/mol×0.000295mol=0.00354g,
合金中C的含量为:
×100%≈0.32%,
由于:0.03%<0.32%<2%,
所以该合金为钢,
答:通过计算可知,该合金为钢.
| 0.013g |
| 44g/mol |
根据质量守恒定律可知合金中C的质量为:12g/mol×0.000295mol=0.00354g,
合金中C的含量为:
| 0.00354g |
| 1.1g |
由于:0.03%<0.32%<2%,
所以该合金为钢,
答:通过计算可知,该合金为钢.
点评:本题考查了混合物反应的计算,题目难度不大,注意质量守恒定律在化学计算中的应用,明确质量分数的概念及表达式,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法正确的是( )
| A、溶液、胶体和浊液的本质区别在于分散质粒子的直径不同 |
| B、金属氧化物都属于碱性氧化物 |
| C、非金属氧化物都属于酸性氧化物 |
| D、氧化还原反应的本质是化合价发生升降 |
下列说法不正确的是( )
| A、溶液、胶体和悬浊液这三种分散系的本质区别是能否透过滤纸或半透膜 |
| B、仅用新制的氢氧化铜悬浊液一种试剂可鉴别乙醇、甘油、乙醛、乙酸、乙酸乙酯、葡萄糖溶液(必要时可加热) |
C、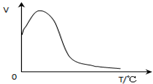 过氧化氢在酶催化作用下的分解反应速率随温度的变化关系如图所示 |
| D、工业上从海带中提取碘单质,经历的步骤有浸泡-过滤-氧化-结晶-粗碘提纯 |
甲乙两个装置中,胶头滴管中吸入某种液体,广口瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则所用试剂可能是( )

| A、甲:NaOH溶液和CO2,乙:H2O2和MnO2 |
| B、甲:CaCl2和Na2CO3溶液,乙:NaOH溶液和Cl2 |
| C、甲:浓硫酸和铝片.乙:浓氨水和SO2 |
| D、甲:浓硫酸和蔗糖.乙:水和氯化氢气体 |
甲、乙两烧杯中各盛有100mL 3mol/L的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后收集到相同条件下气体体积比为甲:乙=1:2,则加入铝粉的质量为( )
| A、5.4g | B、3.6g |
| C、2.7g | D、1.6g |
在2L密闭容器中把4molA和2mol B混合,在一定条件下发生反应3A(g)+2B(g)?zC(g)+2D(g).2min后反应达到平衡时生成1.6mol C,又测得反应速率v(D)=0.2mol/(L?min).则下列说法正确的是( )
| A、z=4 | ||
| B、B物质的转化率是20% | ||
| C、A的平衡浓度是1.6 mol/L | ||
D、平衡时气体压强是原来的
|