题目内容
相同质量的钠、镁、铝分别跟足量稀硫酸反应,在同温同压下产生的气体的体积比为 .
考点:化学方程式的有关计算
专题:
分析:设钠、镁、铝的质量为1g,带入n=
计算物质的量,根据2Na~H2↑、Mg~H2↑、2Al~3H2↑计算生成氢气的物质的量,同温同压下产生的气体的体积比等于物质的量之比.
| m |
| M |
解答:
解:设钠、镁、铝的质量为1g,
n(Na)=
=
mol,由2Na~H2↑可知,生成n(H2)=
×
mol=
mol,
n(Mg)=
=
mol,由Mg~H2↑可知,生成n(H2)=
mol,
n(Al)=
=
mol,由2Al~3H2↑可知,生成n(H2)=
mol×
=
mol,
同温同压下产生的气体的体积比等于物质的量之比=
mol:
mol:
mol=36:69:92,
故答案为:36:69:92.
n(Na)=
| 1g |
| 23g/mol |
| 1 |
| 23 |
| 1 |
| 2 |
| 1 |
| 23 |
| 1 |
| 46 |
n(Mg)=
| 1g |
| 24g/mol |
| 1 |
| 24 |
| 1 |
| 24 |
n(Al)=
| 1g |
| 27g/mol |
| 1 |
| 27 |
| 1 |
| 27 |
| 3 |
| 2 |
| 1 |
| 18 |
同温同压下产生的气体的体积比等于物质的量之比=
| 1 |
| 46 |
| 1 |
| 24 |
| 1 |
| 18 |
故答案为:36:69:92.
点评:本题考查物质的量的有关计算,难度不大,明确2Na~H2↑、Mg~H2↑、2Al~3H2↑的物质的量关系是解题的关键,注意同温同压下产生的气体的体积比等于物质的量之比.

练习册系列答案
相关题目
已知氧化性Fe3+>I2.FeI2溶液中通入一定量的Cl2,发生反应的离子方程式为:a Fe2++bI-+c Cl2→d Fe3++e I2+f Cl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A、2 4 3 2 2 6 |
| B、0 2 1 0 1 2 |
| C、2 0 1 2 0 2 |
| D、2 10 6 2 5 12 |
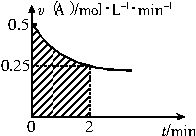 某溶液中发生反应A
某溶液中发生反应A| 无 |
| 无 |
| A、反应开始的前2min,A的平均反应速率小于0.375mol?L-1?min-1 |
| B、图中阴影部分的面积表示0~2min内A的物质的量浓度的减小值 |
| C、图中阴影部分的面积表示0~2min内A的物质的量的减小值 |
| D、至2min时,B的物质的量浓度c(B)介于1~1.5mol?L-1之间 |
把足量的小苏打固体和少量的过氧化钠固体混合均匀后充分加热,最后留下的固体物质的化学式是( )
| A、Na2CO3 |
| B、NaOH和Na2CO3 |
| C、Na2O2和Na2CO3 |
| D、Na2O2、NaOH和Na2CO3 |
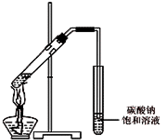 乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某校化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答. A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素.它们之间的关系如下:
A、B、C、D、E、F六种元素,其中A、B、C、D、E为短周期主族元素.它们之间的关系如下: