题目内容
12.下列有关分子晶体熔点高低的叙述中,正确的是( )| A. | 氯气>碘单质 | B. | 四氯化硅>四氟化硅 | ||
| C. | NH3<PH3 | D. | 异戊烷>正戊烷 |
分析 分子晶体是分子间通过分子间作用力(范德华力和氢键)构成的晶体,由于范德华力和氢键,作用力小,氢键作用力大于范德华力,含有氢键的物质熔沸点较高,相对分子质量越大,分子间作用力越强,以此解答该题.
解答 解:A.碘常温下为固体,氯气为气体,碘的熔点较高,故A错误;
B.四氯化硅、四氟化硅对应的晶体都为分子晶体,四氯化硅相对分子质量越大,熔点较高,故B正确;
C.氨气含有氢键,沸点较高,故C错误;
D.同分异构体中,含有的支链越多,沸点越低,故D错误.
故选B.
点评 本题考查晶体熔沸点高低判断,为高频考点,侧重于学生的分析能力的考查,把握影响晶体熔沸点高低的因素是解本题关键,题目难度不大.

练习册系列答案
相关题目
3.下列反应无论怎样调整反应物的用量都只能生成一种物质的是( )
| A. | 甲烷与氯气混合后光照发生反应 | B. | 乙炔与氯气的加成反应 | ||
| C. | 乙烯与氯化氢的加成反应 | D. | 二氧化碳通入石灰水中 |
7.如表各组物质中,不能按a→b→c关系相互转化的是(“→”表示一步完成)( )
| 选项 | a | b | c |
| A | Fe | FeCl3 | FeCl2 |
| B | Na | Na2O2 | NaOH |
| C | Si | SiO2 | H2SiO3 |
| D | HNO3 | NO | NO2 |
| A. | A | B. | B | C. | C | D. | D |
4.在1L含AlCl3、FeCl3、HCl的溶液中,c(Al3+)=0.1mol•L-1,c(Fe3+)=0.2mol•L-1,c(Cl-)=1.2mol•L-1.为了分离出Fe(OH)3,向该溶液中加入2mol•L-1NaOH溶液的体积至少为( )
| A. | 500mL | B. | 600mL | C. | 650mL | D. | 700mL |
8.下列反应中,符合能量变化如图所示的反应是( )
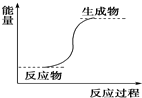

| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝与稀盐酸 | ||
| C. | NaOH与HCl的反应 | D. | 甲烷与O2的燃烧反应 |