题目内容
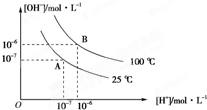 在水的电离平衡中,[H+]和[OH-]的关系如图所示:
在水的电离平衡中,[H+]和[OH-]的关系如图所示:(1)A点水的离子积为1×10-14 mol2?L-2,B点水的离子积为
(2)100℃时,若向溶液中滴加盐酸,能否使体系处于B点位置?为什么?
(3)100℃时,若盐酸中[H+]=5×10-4mol?L-1,则由水电离产生的[H+]是多少?
分析:(1)水的电离过程是吸热的,升高温度,水的电离程度增大,促进电离;
(2)向溶液中滴加盐酸会对水的电离起到抑制作用,但是温度不变,水的离子积不变;
(3)根据溶液中Kw=C(H+)?c(OH-)来计算即可.
(2)向溶液中滴加盐酸会对水的电离起到抑制作用,但是温度不变,水的离子积不变;
(3)根据溶液中Kw=C(H+)?c(OH-)来计算即可.
解答:解:(1)水的电离过程是吸热的,B曲线相当于A曲线在升高温度,则水的电离程度增大,促进电离,所以氢离子和氢氧根离子浓度增大,B曲线下,Kw=C(H+)?c(OH-)=1.0×10-12mol2/L2,水的离子积增大,
故答案为:1×10-12;水的电离过程是吸热的,升高温度,水的电离程度增大,即水的离子积会增大;
(2)向溶液中滴加盐酸会对水的电离起到抑制作用,氢离子浓度增大,氢氧根浓度减小,但是温度不变,水的离子积不变,所以体系不会处于B点位置,会在该温度曲线的基础上向着下方移动,
答:不会;氢离子浓度增大,氢氧根浓度减小,但是温度不变,水的离子积不变;
(3)根据溶液中Kw=c(H+)?c(OH-),100℃时,若盐酸中[H+]=5×10-4mol?L-1,则水电离出的c(H+)=c(OH-)=
mol/L=2×10-9mol/L.
答:由水电离产生的[H+]是2×10-9mol/L.
故答案为:1×10-12;水的电离过程是吸热的,升高温度,水的电离程度增大,即水的离子积会增大;
(2)向溶液中滴加盐酸会对水的电离起到抑制作用,氢离子浓度增大,氢氧根浓度减小,但是温度不变,水的离子积不变,所以体系不会处于B点位置,会在该温度曲线的基础上向着下方移动,
答:不会;氢离子浓度增大,氢氧根浓度减小,但是温度不变,水的离子积不变;
(3)根据溶液中Kw=c(H+)?c(OH-),100℃时,若盐酸中[H+]=5×10-4mol?L-1,则水电离出的c(H+)=c(OH-)=
| 10-12 |
| 5×10-4 |
答:由水电离产生的[H+]是2×10-9mol/L.
点评:本题考查学生对水的离子积常数表达式的理解和掌握,属于对知识的梳理和归纳的题目,难度不大.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
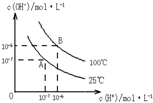 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示: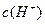 和
和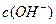 的关系如下图所示:
的关系如下图所示: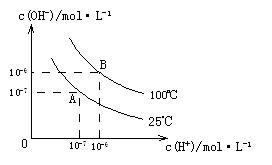
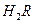 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: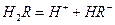 ,
,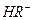

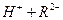 。
。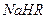 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是: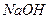 溶液的pH = 。
溶液的pH = 。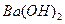 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则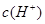 和
和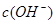 的关系如下图所示:
的关系如下图所示: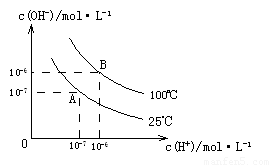
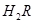 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: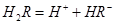 ,
,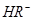
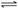
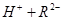 。
。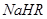 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是: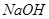 溶液的pH = 。
溶液的pH = 。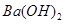 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则