题目内容
8.工业上用电解饱和食盐水的方法制取氢氧化钠、氯气和氢气.但电解前要进行粗盐精制.试回答下列问题:资料卡片:
| 一些物质的溶解性 | ||||
| OH- | Cl- | SO42- | CO32- | |
| H+ | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 | 不 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 微 |
| 杂质 | 加入的试剂 |
| CaCl2 | ⅠNa2CO3 |
| MgCl2 | ⅡNaOH |
| 硫酸盐 | ⅢBaCl2 |
(3)最后加适量的盐酸以调节溶液至中性并除去过量的CO32-.其中盐酸除去CO32-的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O.
分析 (1)在进行粗盐精制时,用Na2CO3除CaCl2,用NaOH除MgCl2,用BaCl2除硫酸盐,据此答题;
(2)镁离子用氢氧根离子沉淀,钙离子用碳酸根离子沉淀,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析;
(3)盐酸与碳酸钠反应生成氯化钠、二氧化碳和水,据此书写化学方程式.
解答 解:(1)在进行粗盐精制时,用Na2CO3除CaCl2,用NaOH除MgCl2,用BaCl2除硫酸盐,所以所加入的试剂为Ⅰ.Na2CO3、Ⅱ.NaOH、Ⅲ.BaCl2,
故答案为:Na2CO3;NaOH;BaCl2;
(2)Ⅰ中加入过量Na2CO3溶液不仅为了完全除去Ca2+,还可以将过量的钡离子沉淀,Ⅰ一定要在Ⅲ之后,
故答案为:Ⅲ;Ⅰ;
(3)盐酸与碳酸钠反应生成氯化钠、二氧化碳和水,反应的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O,
故答案为:Na2CO3+2HCl=2NaCl+CO2↑+H2O.
点评 除杂问题是化学实验中的一类重要问题,除杂时不仅要能把杂质除掉,还不能引入新杂质,而且方法要简便易行,把握好此原则需要我们有扎实的基础知识和缜密的思维.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.向2.0L恒容密闭容器中充入1.0mol PCl5,在温度为T时发生如下反应PCl5(g)?PCl3(g)+Cl2(g)△H=+124kJ•mol-1.反应过程中测定的部分数据见表:
回答下列问题:(1)反应在前50s的平均速率v(PCl5)=0.0016mol/(L•s)
(2)温度为T时,该反应的化学平衡常数=0.025
(3)上述反应到达平衡状态时,PCl3的体积分数为16.7%
要提高平衡时PCl3的体积分数,可采取的措施有CD
A.温度不变,压缩容器体积增大压强 B.使用高效催化剂
C.温度和体积不变,减小PCl5的起始量 D.体积不变,提高反应温度
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=0.1
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是PCl5+4H2O=H3PO4+5HCl.
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
(2)温度为T时,该反应的化学平衡常数=0.025
(3)上述反应到达平衡状态时,PCl3的体积分数为16.7%
要提高平衡时PCl3的体积分数,可采取的措施有CD
A.温度不变,压缩容器体积增大压强 B.使用高效催化剂
C.温度和体积不变,减小PCl5的起始量 D.体积不变,提高反应温度
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a=0.1
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是PCl5+4H2O=H3PO4+5HCl.
3.用”>”、”<”填写下表
| 第一电离能 | 电负性 | 晶格能 | 沸点 |
| O<N | Cl<F | NaCl<CaO | HF>HCl |
17.测定硫酸铜晶体中结晶水含量时,下列情况有可能造成测试结果偏高的是( )
| A. | 加热后在空气中冷却称量固体 | B. | 晶体中含有加热易挥发的杂质 | ||
| C. | 实验所取晶体已有部分脱水 | D. | 晶体加热时脱水不完全 |
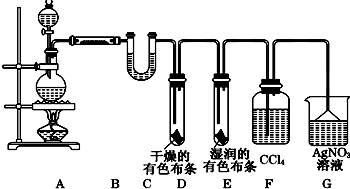
 “低碳经济”已成为科学家研究的主要课题之一.
“低碳经济”已成为科学家研究的主要课题之一.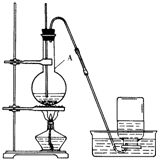
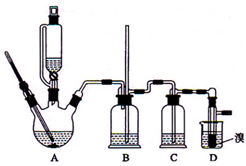 实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:CH2=CH2+Br2→BrCH2CH2Br.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题:
实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:CH2=CH2+Br2→BrCH2CH2Br.可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示.回答下列问题: