题目内容
第四周期金属与人类的生产生活息息相关.
(1)目前市售的发光二极管,其材质以砷化镓(GaAs) 为主.已知镓是与铝同族,镓的基态原子的电子排布式是 .GaAs中Ga的化合价为 .
(2)金属钛坚硬、强度大、耐热、密度小,被称为高技术金属.TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟,则TiCl4属于 (填“原子”“分子”或“离子”)晶体.
(3)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种的化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生白色沉淀; 往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 .
(1)目前市售的发光二极管,其材质以砷化镓(GaAs) 为主.已知镓是与铝同族,镓的基态原子的电子排布式是
(2)金属钛坚硬、强度大、耐热、密度小,被称为高技术金属.TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟,则TiCl4属于
(3)钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种的化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生白色沉淀; 往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为
考点:常见金属元素的单质及其化合物的综合应用
专题:几种重要的金属及其化合物
分析:(1)镓与铝同族,位于周期表第4ⅢA族,原子序数为31,结合构造原理书写电子排布式;
(2)TiCl4在常温下是无色液体,应属于分子晶体;
(3)往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,说明不能电离出SO42-,SO42-为配离子,若加入AgNO3溶液时,产生淡黄色沉淀,说明电离出Br-,Br-为外界离子.
(2)TiCl4在常温下是无色液体,应属于分子晶体;
(3)往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,说明不能电离出SO42-,SO42-为配离子,若加入AgNO3溶液时,产生淡黄色沉淀,说明电离出Br-,Br-为外界离子.
解答:
解:(1)镓与铝同族,位于周期表第4ⅢA族,原子序数为31,最外层有3个电子,最高正价为+3价,电子排布式为1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1),
故答案为:1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1);+3;
(2)TiCl4在常温下是无色液体,熔沸点较低,应属于分子晶体,故答案为:分子;
(3)往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,说明不能电离出SO42-,SO42-为配离子,若加入AgNO3溶液时,产生淡黄色沉淀,说明电离出Br-,Br-为外界离子,则第二种配合物的化学式为[Co(NH3)5SO4]Br,
故答案为:[Co(NH3)5SO4]Br.
故答案为:1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1);+3;
(2)TiCl4在常温下是无色液体,熔沸点较低,应属于分子晶体,故答案为:分子;
(3)往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,说明不能电离出SO42-,SO42-为配离子,若加入AgNO3溶液时,产生淡黄色沉淀,说明电离出Br-,Br-为外界离子,则第二种配合物的化学式为[Co(NH3)5SO4]Br,
故答案为:[Co(NH3)5SO4]Br.
点评:本题考查较为综合,涉及电子排布式、晶体类型以及配合物知识,为高频考点,注意把握电子排布式的书写以及配合物知识,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
下列变化属于加成反应的是( )
| A、乙烯通过酸性KMnO4溶液 |
| B、乙醇和浓硫酸共热 |
| C、乙炔使溴水褪色 |
| D、苯酚与浓溴水混合 |
下列物质在水溶液中的电离方程式不正确的是( )
| A、NaClO?Na++ClO- | ||||||||
B、KHC
| ||||||||
C、NH3?H2O?N
| ||||||||
D、NaHS
|
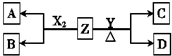 由周期表中前20号元素组成的单质X2、Y和化合物Z的有关信息如下表,X2、Y 和Z之间的转化关系如图(其他无关物质已略去).请回答下列问题:
由周期表中前20号元素组成的单质X2、Y和化合物Z的有关信息如下表,X2、Y 和Z之间的转化关系如图(其他无关物质已略去).请回答下列问题: