题目内容
某元素同位素
X的氯化物XCl21.9g溶于水配成溶液后,需用1mol/L的AgNO3溶液40mL,才能把氯离子完全沉淀下来,已知该同位素中质子数等于中子数,
(1)求算X的质量数是多少?
(2)指出X在周期表中的位置(周期、族).
A Z |
(1)求算X的质量数是多少?
(2)指出X在周期表中的位置(周期、族).
考点:质量数与质子数、中子数之间的相互关系,离子方程式的有关计算
专题:原子组成与结构专题
分析:(1)利用Cl-+Ag+═AgCl↓来计算Cl-的物质的量,从而得出氯化物的物质的量,再利用M=
及摩尔质量与相对分子质量的数值相等来计算;
(2)利用中子数+质子数=质量数,根据原子的构成来分析.
| m |
| n |
(2)利用中子数+质子数=质量数,根据原子的构成来分析.
解答:
解:(1)硝酸银的物质的量为0.04L×1mol?L-1=0.04mol,即银离子的物质的量为0.04mol,
由Cl-+Ag+═AgCl↓可知,硝酸银溶液40mL能把氯离子完全沉淀下来,
则Cl-的物质的量为0.04mol,
XCl2的物质的量为0.02mol,
则XCl2的摩尔质量为
=95g/mol,
其相对分子质量为85,则X的质量数为95-35.5×2=24,
答:X的质量数为24;
(2)已知该同位素中质子数等于中子数,X的质子数为24×
=12,则X为12号元素镁;
Mg为第三周期第VIIA族;
答:X在周期表中的位置为第三周期第VIIA族.
由Cl-+Ag+═AgCl↓可知,硝酸银溶液40mL能把氯离子完全沉淀下来,
则Cl-的物质的量为0.04mol,
XCl2的物质的量为0.02mol,
则XCl2的摩尔质量为
| 1.9g |
| 0.02mol |
其相对分子质量为85,则X的质量数为95-35.5×2=24,
答:X的质量数为24;
(2)已知该同位素中质子数等于中子数,X的质子数为24×
| 1 |
| 2 |
Mg为第三周期第VIIA族;
答:X在周期表中的位置为第三周期第VIIA族.
点评:本题考查学生利用离子反应、质量与物质的量的关系、原子中的数量关系来计算,难度中等,注重对基础知识的考查和训练.

练习册系列答案
相关题目
X、Y、Z是周期表中相邻的三元素,X和Y同周期,Y和Z同主族,三原子的最外层电子数之和为14,质子数之和为28,则三元素为( )
| A、N、P、O |
| B、N、C、Si |
| C、B、Mg、Al |
| D、C、N、P |
下列曲线表示卤素元素某种性质随核电荷数的变化趋势,正确的是( )
A、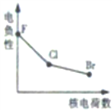 |
B、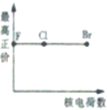 |
C、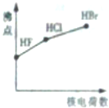 |
D、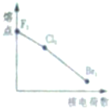 |
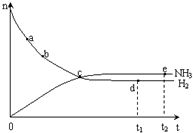 合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0
合成氨工业对国民经济和社会发展具有重要的意义. 合成塔中发生反应为:N2(g)+3H2(g)?2NH3(g)△H<0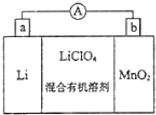 锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
锰锂电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题: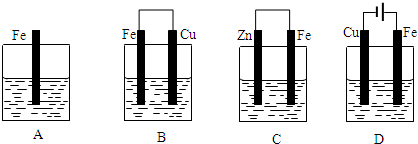
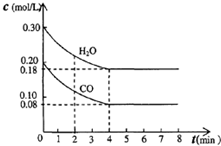 (1)氢能是高效、清洁能源,制氢技术的研究开发是氢能利用的必由之路.燃料水蒸气重整法是一种有效、经济、广泛采用的制氢方法,它是通过水蒸气与燃料间的反应来制取氢气的.①在催化剂作用下,天然气和水蒸气反应可制得一氧化碳和氢气,已知该反应每制得1kg氢气需要吸收3.44×104 kJ热量,请写出该反应的热化学式:
(1)氢能是高效、清洁能源,制氢技术的研究开发是氢能利用的必由之路.燃料水蒸气重整法是一种有效、经济、广泛采用的制氢方法,它是通过水蒸气与燃料间的反应来制取氢气的.①在催化剂作用下,天然气和水蒸气反应可制得一氧化碳和氢气,已知该反应每制得1kg氢气需要吸收3.44×104 kJ热量,请写出该反应的热化学式: