题目内容
18.设NA表示阿伏加德罗常数,下列说法不正确的是( )| A. | NA个氢分子与NA个氧分子的质量比为1:1 | |
| B. | 1 mol氢气的质量与NA个氢分子的质量相等 | |
| C. | 16g氧气中含有的氧原子数为NA | |
| D. | 44g CO2与28g CO所含有的分子数均为NA |
分析 A、NA个氢分子与NA个氧分子的物质的量均为1mol,而物质的量相同时,质量之比等于摩尔质量之比;
B、1mol氢气中含NA个氢气分子;
C、氧气由氧原子构成;
D、求出二氧化碳和CO的物质的量,然后根据分子个数N=nNA来分析.
解答 解:A、NA个氢分子与NA个氧分子的物质的量均为1mol,而物质的量相同时,质量之比等于摩尔质量之比,故氢气和氧气的质量之比为2:32=1:16,故A错误;
B、1mol氢气中含NA个氢气分子,故1mol氢气的质量和NA个氢气分子的质量相同,故B正确;
C、氧气由氧原子构成,故16g氧气中含有的氧原子的物质的量为1mol,故含NA个,故C正确;
D、44g二氧化碳和28gCO的物质的量均为1mol,故分子个数N=nNA=NA个,故D正确.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列实验装置设计正确、且能达到目的是( )
| A. | 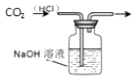 用于除去CO2中的HCl | B. | 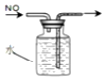 排水法收集NO | ||
| C. | 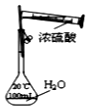 配制一定物质的量浓度的稀硫酸 | D. | 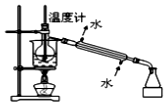 海水的淡化 |
9.某原子的摩尔质量是Mg•mol-1,则一个该原子的真实质量是( )
| A. | $\frac{M}{6.02×1{0}^{23}}$g | B. | $\frac{1}{M}$ g | C. | M g | D. | $\frac{6.02×1{0}^{23}}{M}$ g |
6.下列离子方程式书写正确的是( )
| A. | 石灰石与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 醋酸与烧碱溶液反应:H++OH-═H2O | |
| C. | MgSO4溶液与Ba(OH)2溶液反应:SO42-+Ba2+═BaSO4↓ | |
| D. | 硫酸与氨水混合:H++NH3•H2O═NH4++H2O |
3.下列物质属于醇类的是( )
| A. | 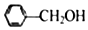 | B. | 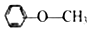 | C. | 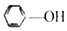 | D. | 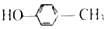 |
10.下列说法正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质溶液的强 | |
| B. | 氧化钠是强电解质,醋酸是弱电解质 | |
| C. | 氨气是弱电解质,铜是强电解质 | |
| D. | 硫酸钠是强电解质,硫酸钡是弱电解质 |
7.在如图所示的装置中,a的金属活动性比氢强,b为碳棒,关于此装置的各种叙述不正确的是( )

| A. | 碳棒上有气体放出,溶液pH变大 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,电子从a极流向b极 | |
| D. | a极上发生了氧化反应 |
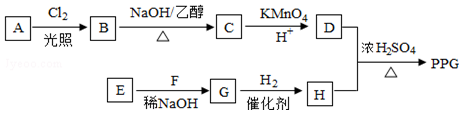
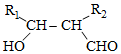
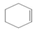 在酸性高锰酸钾溶液中反应生成HOOCCH2CH2CH2CH2COOH
在酸性高锰酸钾溶液中反应生成HOOCCH2CH2CH2CH2COOH .
. .
.
 :
: