题目内容
下列各项中,理由、结论及因果关系均正确的是( )
| A、由于键能EN≡N>ECl-Cl,故单质的沸点:N2>Cl2 |
| B、由于分子中可电离的H+个数H2SO4>CH3COOH,故两者的酸性:H2SO4>CH3COOH |
| C、由于元素的非金属性N>P,故氢化物的稳定性:NH3>PH3 |
| D、由于金属性Fe>Cu,故还原性Fe2+>Cu |
考点:不同晶体的结构微粒及微粒间作用力的区别,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A、一般来说分子晶体熔沸点与相对分子量成正比;
B、酸性的强弱取决与电离程度的大小,而不是氢离子的个数;
C、非金属性越强,氢化物的稳定性越强;
D、根据阳离子的氧化性越强,对应的原子或阳离子的还原性越弱.
B、酸性的强弱取决与电离程度的大小,而不是氢离子的个数;
C、非金属性越强,氢化物的稳定性越强;
D、根据阳离子的氧化性越强,对应的原子或阳离子的还原性越弱.
解答:
解:A、Cl2的相对分子质量大于N2,所以单质沸点:Cl2>N2,故A错误;
B、H2SO4是强酸,CH3COOH弱酸,所以酸性:H2SO4>CH3COOH,故B错误;
C、元素的非金属性:N>P,所以稳定性:NH3>PH3,故C正确;
D、氧化性:Fe 3+>Cu2+,还原性:Cu>Fe2+,故D错误;
故选C.
B、H2SO4是强酸,CH3COOH弱酸,所以酸性:H2SO4>CH3COOH,故B错误;
C、元素的非金属性:N>P,所以稳定性:NH3>PH3,故C正确;
D、氧化性:Fe 3+>Cu2+,还原性:Cu>Fe2+,故D错误;
故选C.
点评:本题主要考查了物质性质的比较,熟悉非金属性、单质沸点、还原性的比较方法即可解答,难度不大.

练习册系列答案
相关题目
下列反应中属于吸热反应的是( )
| A、Ba(OH)2?8H2O(s)+NH4Cl(s) |
| B、酸碱中和反应 |
| C、铝热反应 |
| D、实验室制取氢气的反应 |
下列物质中所含分子物质的量最多的是( )
| A、44 g CO2 |
| B、1.5 mol H2 |
| C、64 g SO2 |
| D、3.01×1023个硫酸分子 |
我国歼-10战斗机利用现代科技将
Po涂于飞机表面,可以吸收和屏蔽雷达和红外线辐射,起到一定的隐身作用.该Po(钋)原子核外电子数是( )
209 84 |
| A、209 | B、125 |
| C、84 | D、42 |
下列表达式错误的是( )
A、甲基的电子式: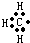 |
B、碳原子的价电子轨道表示式: |
| C、硫离子的核外电子排布式:1s22s22p6 |
| D、碳-14原子:614C |
 在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0
在一容积为2L的密闭容器中,加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)?2NH3(g)△H<0 镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用
镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用 .请写出A与稀、冷的KMnO4溶液在碱性
.请写出A与稀、冷的KMnO4溶液在碱性