题目内容
9.关于如图所示的原电池,下列说法正确的是( )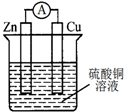
| A. | 电子从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 反应后,锌电极的质量减小 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
分析 该原电池中,Zn易失电子作负极、Cu作正极,正极电极反应式为Cu2++2e-=Cu,负极电极反应式为Zn-2e-=Zn2+,电子从负极沿导线流向正极,盐桥中阳离子向正极移动、阴离子向负极移动,据此分析解答.
解答 解:A.锌作负极、铜作正极,电子从锌电极通过电流计流向铜电极,故A正确;
B.Zn易失电子作负极,发生氧化反应,Cu作正极,发生还原反应,故B错误;
C.Zn易失电子作负极,溶解,质量减小,故C正确;
D.铜电极上铜离子得电子发生还原反应,电极反应式为Cu2++2e-=Cu,故D错误.
故选AC.
点评 本题考查了原电池原理,明确正负极上发生的反应、电子及离子移动方向即可解答,题目难不大.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
19.下列关于离子化合物的叙述正确的是( )
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 离子化合物一定可以导电 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
17.常温下将稀KOH溶液和稀CH3COOH溶液混合,不可能出现的结果是( )
| A. | pH>7,且c(OH?)>c(K+)>c(H+)>c(CH3COO?) | B. | pH>7,且c(K+)+c(H+)=c(CH3COO?)+c(OH?) | ||
| C. | pH<7,且c(CH3COO?)>c(H+)>c(K+)>c(OH?) | D. | pH=7,且c(CH3COO?)=c(K+)>c(H+)=c(OH?) |
4.下列各指定微粒的数目比是1:1的是( )
| A. | Na2O2溶液中阴离子和阳离子 | |
| B. | NaHSO4溶液中阳离子和阴离子 | |
| C. | ${\;}_{12}^{24}$Mg2+离子中的质子和中子 | |
| D. | 氯化钠溶液中阳离子和阴离子的电子数 |
14.能源可分为一级能源和二级能源.下列叙述正确的是( )
| A. | 水煤气是一级能源 | B. | 天然气是二级能源 | ||
| C. | 电能是二级能源 | D. | 水力是二级能源 |
1.下列A、B两种元素,其中可以组成AB2型离子化合物的是( )
| A. | C和O | B. | Na和S | C. | Mg和Cl | D. | Ne和O |
18.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 还原性强弱:CI-<Br一<I - | B. | 微粒半径大小:S>Na+>O2- | ||
| C. | 热稳定性:HF>H2O>NH3 | D. | 碱性:KOH>NaOH>LiOH |
19.光照对下列反应几乎无影响的是( )
| A. | 氢气与氯气 | B. | 溴化银的分解 | C. | 甲烷与氧气 | D. | 次氯酸分解 |