题目内容
下列因果关系叙述正确的是( )
| A、SO2具有漂白性,故可使酸性KMnO4溶液褪色 |
| B、浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| C、Na的金属性比Cu强,故可用Na与CuSO4溶液反应制取Cu |
| D、Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中Fe也显+3价 |
考点:硝酸的化学性质,二氧化硫的化学性质,钠的化学性质,铁的化学性质
专题:元素及其化合物
分析:A.SO2使酸性KMnO4溶液褪色体现了二氧化硫的还原性;
B.HNO3见光会分解生成的二氧化氮;
C.Na投入到CuSO4溶液,先与水发生反应生成氢氧化钠,氢氧化钠再与硫酸铜发生复分解反应;
D.Fe在硫中加热生成硫化亚铁.
B.HNO3见光会分解生成的二氧化氮;
C.Na投入到CuSO4溶液,先与水发生反应生成氢氧化钠,氢氧化钠再与硫酸铜发生复分解反应;
D.Fe在硫中加热生成硫化亚铁.
解答:
解:A.SO2具有漂白性,但是二氧化硫使酸性KMnO4溶液褪色,是因为二氧化硫的还原性,与漂白性无关,故A错误;
B.HNO3见光会分解生成的二氧化氮,二氧化氮溶于硝酸显黄色,故B正确;
C.Na投入到CuSO4溶液,先与水发生反应生成氢氧化钠,氢氧化钠再与硫酸铜发生复分解反应,故C错误;
D.Fe在硫中加热生成硫化亚铁,故D错误;
故选:B.
B.HNO3见光会分解生成的二氧化氮,二氧化氮溶于硝酸显黄色,故B正确;
C.Na投入到CuSO4溶液,先与水发生反应生成氢氧化钠,氢氧化钠再与硫酸铜发生复分解反应,故C错误;
D.Fe在硫中加热生成硫化亚铁,故D错误;
故选:B.
点评:本题考查了二氧化硫、硝酸、钠、氯气的性质,侧重考查学生对基础知识掌握的熟练程度,题目难度不大,注意氯气具有强的氧化性,与变价金属反应均生成高价态的氯化物.

练习册系列答案
相关题目
已知一定条件下,CO2 和CO的混合气体对氢气的相对密度是20,则CO2 和CO的质量比为( )
| A、1:3 | B、33:7 |
| C、3:1 | D、7:33 |
 电子产品小型化、微型化、集成化是当今世界技术发展的大势所趋,对锂离子二次电池提出了更高比容量的要求,锂硫电池的理论能量密度为是锂离子二次电池的3-5倍,是极具应用前景的电化学储能体系,近年来引起了研究人员的广泛关注.锂硫电池常用有机溶剂碳酸酯类(
电子产品小型化、微型化、集成化是当今世界技术发展的大势所趋,对锂离子二次电池提出了更高比容量的要求,锂硫电池的理论能量密度为是锂离子二次电池的3-5倍,是极具应用前景的电化学储能体系,近年来引起了研究人员的广泛关注.锂硫电池常用有机溶剂碳酸酯类(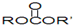 )作为电解质溶液,放电时某极的电极反应式为:S+2Li+2e-═Li2S,电池如图所示:图中①②曲线为Li+移动方向.以下说法不正确的是( )
)作为电解质溶液,放电时某极的电极反应式为:S+2Li+2e-═Li2S,电池如图所示:图中①②曲线为Li+移动方向.以下说法不正确的是( )| A、放电时Li+移动方向与曲线①一致 |
| B、电解质溶液不能用醋酸溶液代替碳酸酯类 |
| C、充电时阴极反应式:Li++e-═Li |
| D、充电时b电极接电源的正极 |
化学无处不在,下列与化学有关的说法不正确的是( )
| A、“日照香炉生紫烟”的“烟”是瀑布的细小水珠形成的水雾,属于胶体 |
| B、“大漠孤烟直”的“烟”是燃烧柳枝时产生的烟,这类染料在燃烧过程中会产生污染空气的烟雾 |
| C、“月朦胧,鸟朦胧,空气雾霾浓.山朦胧,树朦胧,喉咙有点痛”,二氧化硫、氮氧化合物以及可吸入颗粒物是雾霾的主要组成,而前两项主要来自于汽车尾气的排放 |
| D、“塞翁失马焉知非福”说的是用辩证的观点看待事物,一分为二,比如SO2虽然是空气污染气体之一,但也可以被用于消毒杀菌 |
化学与生产和生活密切相关,下列说法正确的是( )
| A、金属钠可以保存在煤油或酒精中,防止在空气中变质 |
| B、石油的裂化和煤的干馏,都属于化学变化 |
| C、等质量的葡萄糖和果糖在人体内完全氧化释放的能量相等 |
| D、聚氯乙烯制品易造成白色污染,可采用焚烧法处理 |
如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O下列关于该电池工作时说法正确的是( )


| A、甲池中负极反应为:N2H4-4e-═N2+4H+ |
| B、甲池溶液pH不变,乙池溶液pH减小 |
| C、甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体 |
| D、反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度 |
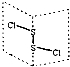 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )| A、S2Cl2的结构中各原子均达到8电子的稳定结构 |
| B、S2Cl2为含有极性键和非极性键的共价化合物 |
| C、若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2 |
| D、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
下列离子方程式书写正确的是( )
| A、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ |
| B、NaHS溶液呈碱性:H3O++HS-?H2S+H2O |
| C、4mol/L的KAl(SO4)2溶液与7mol/L的Ba(OH)2溶液等体积混合:4Al3++7SO42-+7Ba2++14OH-═2Al(OH)3↓+2AlO2-+7BaSO4↓+4H2O |
| D、氯气溶于水:Cl2+H2O═2H++Cl-+ClO- |